京都大学iPS细胞研究所(CiRA)的本池总太特命助教、池谷真教授、稻田与志子(技术职员)、户口田淳也特定据点教授以及广岛大学医院口腔检查中心的加治屋干人教授等人的研究团队宣布,利用人iPS细胞重现发育过程,成功制备出了颌骨类器官。将该类器官移植到小鼠体内后,出现了血管新生并形成了成熟的骨组织。同时研究还证实,利用罕见病——骨形成不全症患者来源的iPS细胞,能够再现该病的病理状态。上述研究成果有望推动开发出针对产生颌骨异常的病变的治疗方法。相关研究成果已发表在期刊《Nature Biomedical Engineering》的7月2日刊上。
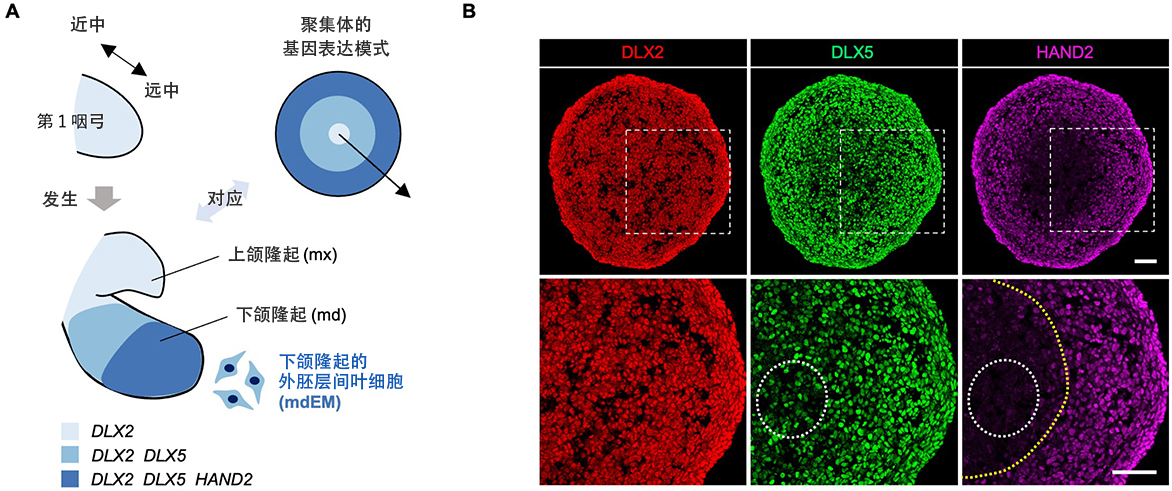
图1 下颌隆起外胚层间叶细胞(mdEM)的诱导(供图:京都大学)
A:第1咽弓的近中侧分化为上颌隆起,远中侧分化为下颌隆起。基因表达模式因区域而异。
B:利用结果1)中制作的神经嵴细胞进一步诱导形成的聚集体的免疫染色图像。图为iPS细胞分化第9天的状态。比例尺为100μm(0.1毫米)。
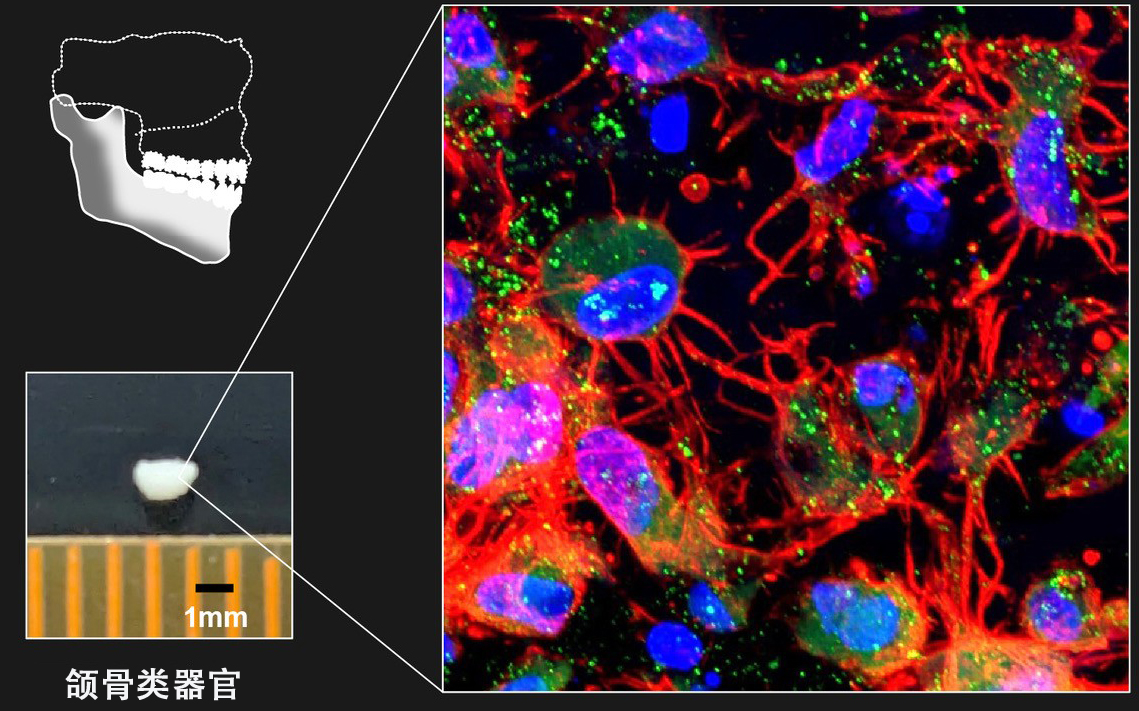
图2 利用人类iPS细胞诱导颌骨类器官(供图:京都大学)
A:iPS细胞分化第38天的聚集体状态。
B:颌骨类器官的免疫染色图像。成熟骨细胞(SOST)与肌动蛋白纤维(Phalloidin)的状态。比例尺为100μm(0.1毫米)。
颌骨由上颌骨和下颌骨构成,当因细菌感染、过度负荷、肿瘤等原因遭到大规模破坏时,其愈合与功能的恢复就会变得极为困难,目前仍存在许多病理状态不明的难治症状。
全身的主要骨骼来源于中胚层系统,而颌骨来源于神经嵴细胞(NCCs),由神经嵴细胞迁移至第1咽弓后,经过向外胚层间叶(PA1-EM)的分化而形成。此外,已知主要骨骼以软骨原基逐渐被骨组织替代的软骨内成骨方式(内骨化)形成,而颌骨则以不经过软骨形成而由聚集的细胞直接形成骨组织的膜内成骨方式形成。然而此前,不仅是颌骨,对于功能发挥至关重要的骨细胞三维网络结构的再现尚未实现,向PA1-EM的诱导方法也尚未确立。
为此,研究团队探讨了利用iPS细胞诱导具有三维结构的颌骨类器官。同时,考虑到未来的临床应用,还期待能够开发出一种可在不含动物源成分及血清的条件下实现诱导的方法。
已知在发育过程中,神经嵴细胞(NCCs)迁移至哪个区域是由HOX基因的表达模式决定的,迁移至第1咽弓的NCCs未表达HOX基因。此外,第1咽弓会分化为未来形成上颌的上颌隆起和形成下颌的下颌隆起两部分,其中下颌隆起的NCCs会分化为层状表达DLX2、DLX2与DLX5、以及DLX2与DLX5与HANDS2的外胚层间叶(mdEM)。
为此,研究团队开发了立体培养人iPS细胞,将其诱导为未表达HOX基因的NCCs的方法。
对iPS细胞诱导第5天获得的直径约500微米(μm)的细胞团块进行基因表达检测后发现,其大部分由NCC构成,且未表达HOX基因。此外,该细胞团块还再现了在中心部表达DLX2、周围区域表达DLX2与DLX5,更外围区域则呈现DLX2与DLX5与HANDS2的表达模式。
对该细胞团块进行骨分化诱导后,在iPS细胞诱导的第38天,成功获得了大小约1.5毫米米粒状、富含骨相关蛋白质的下颌骨类器官。经确认,所获得的下颌骨类器官高度钙化,含有成骨细胞,并且再现了骨细胞的三维网络结构。
为验证该下颌骨类器官的功能,研究团队在免疫缺陷小鼠的下颌骨上制造了直径为2毫米的缺损,然后移植了3个制备的下颌骨类器官,并与骨移植组、未移植组进行了比较。
移植4周后的显微CT发现,移植了颌骨类器官的缺损部位,其闭合程度与骨移植组相当,组织学上也确认,缺损部位内部伴随着血管新生实现了再生。而未移植组则一直处于缺损状态。
最后,研究团队验证了能否利用颌骨类器官再现疾病。他们分别使用了重症骨形成不全症患者来源的iPS细胞,以及修复了该疾病致病基因突变后的患者来源iPS细胞,分别诱导出了颌骨类器官。
结果显示,患者来源的颌骨类器官基质中含有大量变性胶原蛋白,再现了骨细胞网络受损的病变。而在已修复突变的患者来源类器官中,未观察到这些病变。
该研究目前仍处于基础阶段,未来将进一步进行改良。
本池特命助教表示:“虽然我们制备出的颌骨类器官与普通细胞相比已相当坚硬,但其成熟度仍然较低,未来提高其成熟度也是一项亟待解决的课题。”
原文:《科学新闻》
翻译:JST客观日本编辑部
【论文信息】
期刊:Nature Biomedical Engineering
论文:Jawbone-like organoids generated from human pluripotent stem cells
DOI:10.1038/s41551-025-01419-3