筑波大学人类综合科学研究科生命系统医学专业的坂本和雄(现为神户大学特定助教)与川西邦夫助教(现为昭和医科大学教授)、筑波大学生存动力学研究中心的金俊达助教(现为富山大学副教授)、东海大学医学部的松阪泰二教授等人的研究团队宣布,已解明左右肾脏试图维持功能性与结构性平衡现象(肾脏相互平衡)的分子机制。该发现是通过开发并分析能在左右肾脏中仅单侧诱导损伤的小鼠模型而得出的结论。研究表明,血管紧张素Ⅱ(AngII)的非对称局部激活可能是肾脏相互平衡的成因之一。该成果有望推动肾脏疾病治疗方法的开发。相关研究成果已发表在期刊《日本学士院纪要B》6月20日刊上。
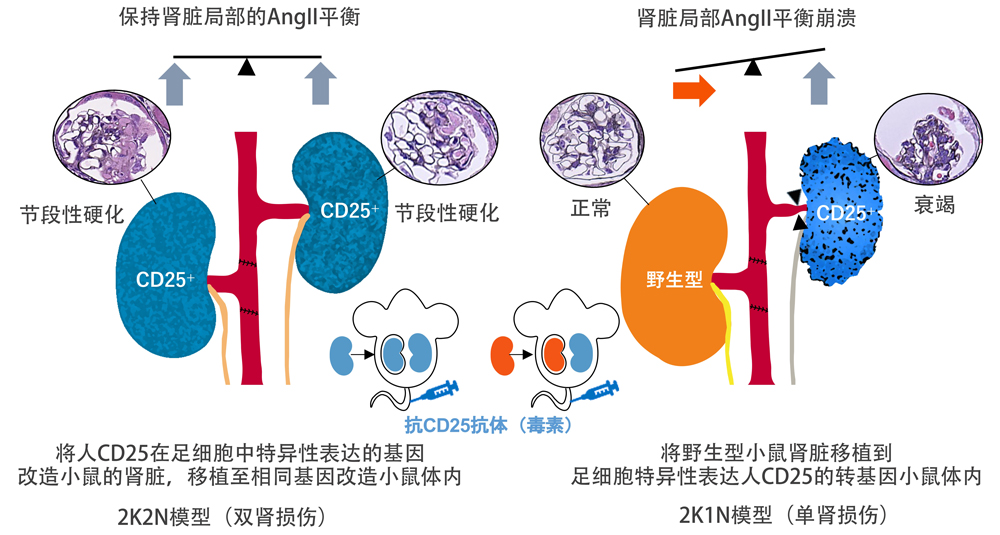
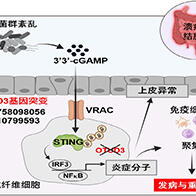
图1 研究成果的概要(提供:神户大学)
肾脏是一对左右成对的器官,当一侧肾脏受损时,受损肾脏会逐渐出现血流下降和结构性萎缩,而对侧肾脏会表现出代偿性的功能亢进和肥大。这种左右肾脏之间的动态平衡调节被称为肾脏相互平衡。但其机制长期以来未被阐明。
慢性肾脏病由衰老、高血压、糖尿病等多种主要因素引发,病情的进展会导致肾功能不可逆地下降,进而需要透析或肾移植。全球的慢性肾病患者呈增加趋势,近年来,早期诊断和干预的重要性逐渐得到重视。
在肾脏疾病的研究中,以往一直使用对单侧肾小管间质施加损伤以再现疾病的动物模型。但这种模型在研究由肾小球引起的病变,以及将左右肾脏视为可能相互影响的系统的肾脏疾病方面存在局限。
为此,本次研究团队制作了向小鼠肾小球细胞施加选择性损伤、且仅在单侧肾脏诱导足细胞(肾脏肾小球表面的上皮细胞)损伤的2K1N模型。
具体而言,研究人员使用肾小球足细胞特异性地表达人CD25的NEP25小鼠(肾病综合征模型),通过施用针对CD25的免疫毒素LMB2,制作了仅在单侧肾脏诱导足细胞损伤(肾小球病,glomerulopathy)的2K1N小鼠模型。
当使用该模型仅对单侧肾脏诱导损伤时,观察到受损肾脏的肾血流呈时间依赖性下降,源自受损肾脏的蛋白尿消失。与此相对,另一侧健康肾脏代偿性地承担起维持功能,全身的水盐平衡和血压得以维持并趋于稳定。
另一方面,在双侧肾脏受到同等损伤的2K2N模型中,未观察到血流不均衡,全身性水肿和蛋白尿情况恶化。
研究团队进一步使用2K1N模型,详细调查肾脏内的基因表达及分子水平变化后发现,在受损肾脏和健康肾脏之间,与升高血压的激素AngII生成相关的蛋白水解酶“肾素Ren1”的表达存在明显的左右差异,肾脏AngII的表达量也在受损肾脏一侧显著增加。
针对这一情况,施用血管紧张素转换酶抑制剂后,血流下降和肾小球病变得到改善,表明这种局部的AngII不均衡引起了受损肾脏的血流下降和肾小球衰竭。
研究发现,在左右肾脏试图相互保持平衡的过程中,该平衡的崩溃与肾脏疾病的进展密切相关。
川西教授表示:“该研究始于筑波大学长田道夫教授(当时)的提议。当时还是研究生的坂本和雄成功完成了使用转基因小鼠进行的高难度病变肾脏移植,并由此发现了在正常肾脏和受损肾脏之间发生了信息交流(串扰)。特别是,肾脏为保护身体而激活肾素-血管紧张素系统(RAS)的新功能得以阐明,目前研究已拓展到移植肾脏的领域。”
原文:《科学新闻》
翻译:JST客观日本编辑部
【论文信息】
期刊:Proceedings of the Japan Academy, Series B
论文:A Novel Glomerulopathy Model Demonstrates Renal Counterbalance via Local Angiotensin II Regulation
DOI:10.2183/pjab.101.025