宫崎大学终身教职推进室的福永圭佑副教授、九州大学研究生院农学研究院的寺本岳大助教、角田佳充教授、冲绳科学技术大学院大学(OIST)核酸化学与工程单元的横林洋平教授、东京科学大学地球生命研究所的松浦友亮教授等宣布,成功运用X射线晶体结构分析方法,阐明了所开发的两种人工RNA-蛋白质复合体(RNP)在结合模式上的差异。研究团队利用这两种RNP成功开发出了高性能核糖开关(用于基因表达调控的RNA开关),并在无细胞蛋白质合成系统(cell-free系统)中验证了其优异性。相关研究成果已发表在国际学术期刊《Nucleic Acids Research》的3月23日刊上。
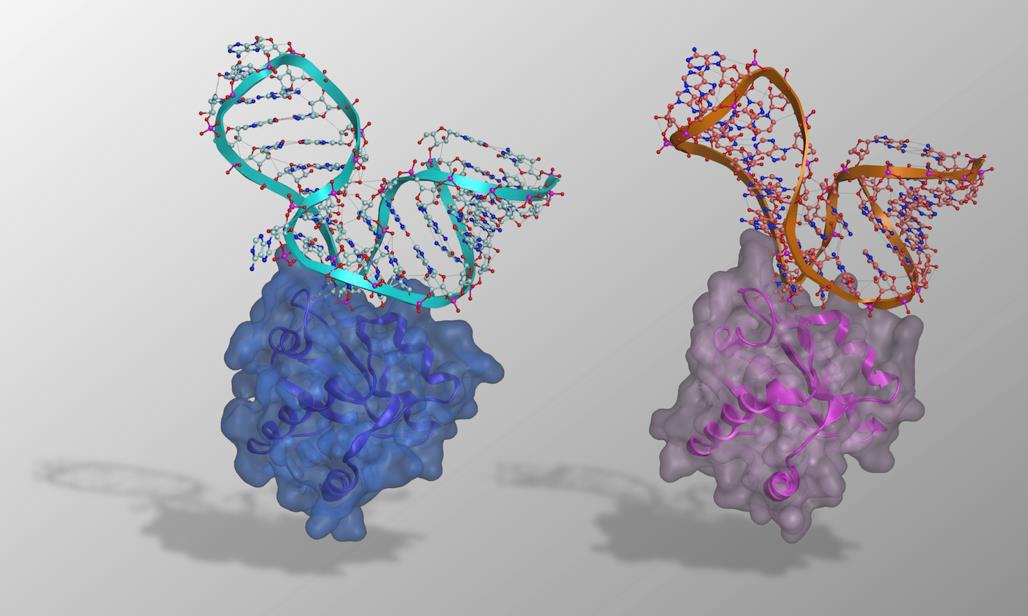
图1. CS1-LS4(左)、CS2-LS12(右)的结构示意图(供图:宫崎大学)
无细胞蛋白质合成系统作为以医疗用途等为目标的特定蛋白质大量合成,以及作为生命化学研究的工具,相关研究正在全球范围内推进。
mRNA结合蛋白在mRNA由细胞核内的DNA转录而来,并在核糖体翻译的过程中发挥着核心作用。
此前,OIST的研究团队开发出了能够改变RNA-RBP间结合模式的PD-SELEX法。通过改造合成生物学研究中通常用作分子元件的古细菌来源L7Ae蛋白及其所结合的kink-turn RNA的结合选择性,成功获得了两组正交性RNA-RBP配对——CS1-LS4与CS2-LS12。另一方面,这些高同源性的RNA-RBP配对能够形成特异性配对的机制此前尚不明确。
对此,研究团队采用X射线共晶结构分析技术,尝试明确其相互作用机制。
研究团队成功确定了CS1-LS4和CS2-LS12的结构。并发现了这两组RNP的整体结构与作为其祖先的kink-turn RNA-L7Ae复合体高度相似。
此外,研究团队还探讨了在无细胞转录翻译系统中发挥作用的蛋白质配体响应型核糖开关的开发。
在T7启动子序列后立即嵌入RNA适配体序列(CS1或CS2),设计出一种在无蛋白质配体(LS4或LS12)条件下通过遮蔽核糖体识别序列以抑制下游基因翻译的机制,制作了仅在配体存在条件下进行蛋白质合成的ON开关。
为验证其性能,研究团队以荧光蛋白(EGFP)报告基因的表达水平为指标开展筛查,确认该无细胞核糖开关具备可与ON/OFF比500相媲美的全球最高性能。据悉,在相关领域中,三位数的ON/OFF比尚无先例。
此外,研究团队利用开发的两种核糖开关,构建了调控γ-溶血素功能表达的逻辑电路(与门电路),并证实该电路可正常运行。
据悉,未来研究团队将进一步提升ON/OFF比,并验证RNA-RBP配对能否在大肠杆菌等不同生物平台中发挥作用。
福永副教授表示:“此次,我们成功解析了通过人工进化(PD-SELEX)获得的超高亲和性RNA-蛋白质(RNP)配对结构,并开发出利用RNP元件的无细胞系统高性能翻译开关。今后,我们还将致力于开发可在细胞内发挥作用的RNA器件。”
原文:《科学新闻》
翻译:JST客观日本编辑部
【论文信息】
期刊:Nucleic Acids Research
论文:Structural insights into lab-coevolved RNA-RBP pairs and applications of synthetic riboswitches in cell-free system
DOI:10.1093/nar/gkaf212