东京大学研究生院农学生命科学研究科的喜田聪教授和日本国立精神与神经医疗研究中心精神保健研究所的金吉晴所长、堀弘明室长等人组成的研究团队发表研究成果称,明确了创伤后应激障碍(PTSD)的分子机制。该研究对PTSD患者的外周血和PTSD模型小鼠的海马区基因表达进行了全面比较,发现两者均出现了cAMP信号传递途径的负调控因子——磷酸二酯酶4B(PDE4B)的表达下降现象。研究还证实,患者体内该因子的表达量越低,再体验症状越严重,而模型小鼠则会因为cAMP信号传递途径的活化而强化创伤记忆。该研究有望为开发PTSD的诊断和治疗方法等提供帮助。相关研究成果已于2月27日发表在国际学术期刊《Molecular Psychiatry》上。
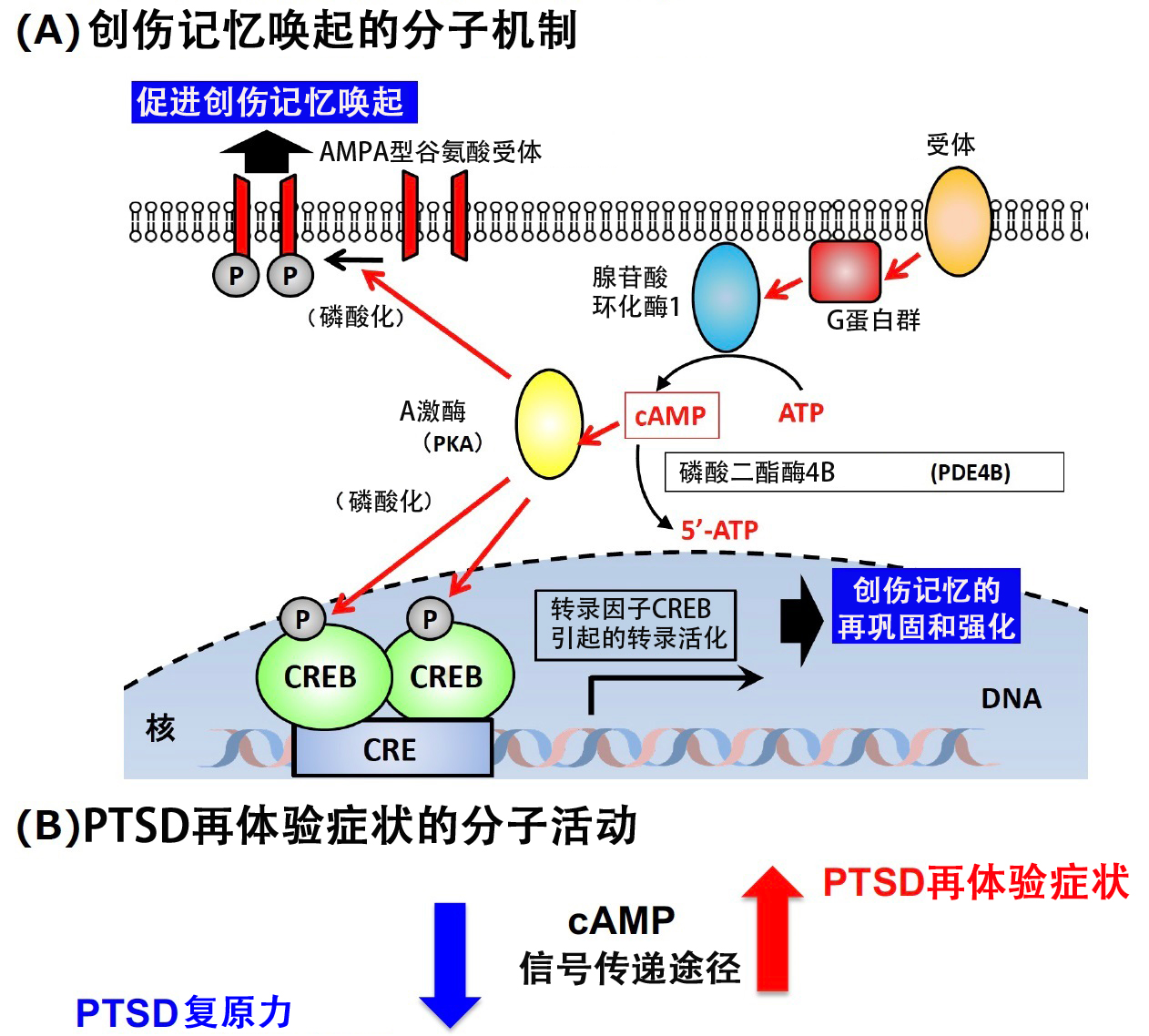
图1:本研究中提出的PTSD再体验症状的分子机制(供图:东京大学)
(A)基于迄今为止的研究成果(长谷川等,Nat Commun., 2019)和本研究成果的创伤记忆唤起的分子机制
(B)cAMP信号传递途径的过度活化引发的PTSD再体验症状发作
PTSD是一种在经历了生死攸关的创伤体验后发作的精神疾病,主要症状包括再体验症状(闪回:创伤记忆唤起的症状)和回避、过度觉醒等,其中再体验症状作为PTSD特有的症状而为人所知。
近年来,利用创伤体验的代表例子——恐惧记忆在动物中普遍存在这一点,把以啮齿动物为中心开展的恐惧记忆相关研究成果应用于PTSD治疗的研究正在不断推进。然而由于PTSD的发病机制不明,目前尚无治疗药物,医生只能开出缓解症状的药物。
此次研究团队为了揭示PTSD的分子机制,特别针对具有强烈再体验症状的PTSD患者和PTSD模型小鼠海马区恐惧记忆唤起时的mRNA表达进行了全面比较。PTSD模型小鼠通过恐惧情境条件学习,形成了将其置于箱子中便会唤起恐惧(创伤)记忆并表现出恐惧反应(无法移动)的条件性恐惧。恐惧反应的程度用5分钟内恐惧反应的持续时间来评价。
研究人员对患者与模型小鼠两者体内相对于健康状态而言表达量发生变化的遗传基因进行搜索后,发现PDE4B的表达出现降低。该基因负责编码分解cAMP的酶,其表达下调意味着cAMP信号传递途径的活化。
此外,研究人员还调查了患者外周血的mRNA表达水平与再体验症状严重程度之间的关系,结果发现mRNA的表达水平越高,再体验症状的严重程度就越严重。同时,研究还表明患者外周血PDE4B基因的甲基化与mRNA表达水平存在相关性,而且表达降低可以是持续性的。当模型小鼠的恐惧记忆被唤起时,不仅海马区,外周血中的PDE4BmRNA的表达量也降低了。这一结果证实,患者和模型小鼠间具有高度同源性。
接着,研究人员对恐惧记忆与cAMP信号传递途径活化的关联进行了验证。此前,该研究团队已经成功揭示了cAMP对记忆的巩固和唤起等方面的重要性。
利用光遗传学方法,研究人员在小鼠大脑中构建了一个通过光照人为增加cAMP数量的试验系统,并以此研究了cAMP增加对恐惧记忆的影响。
结果显示,增加了cAMP的小鼠在恐惧记忆唤起时,恐惧反应变强。并且,如果24小时后再次唤起恐惧记忆,即使不增加cAMP,恐惧反应也会变得更强烈,导致病情加重。实验中还观察到了类似再体验症状的行为。
反之,研究人员构建了一个增加PDE4B降低cAMP的试验系统,结果发现恐惧反应降低,恐惧记忆的再巩固也被抑制。在恐惧记忆唤起前,研究人员将研究团队开发的药物NB001——一种作为慢性疼痛治疗药物而开发的(正在进行临床试验)降低cAMP的药物投用给模型小鼠,也得到了同样的结果。
这些结果表明,cAMP的过度活化是PTSD再体验症状加重的分子活动。
为诊断和治疗方法的开发铺平道路
喜田教授表示:“通过该研究,我们揭示了PTSD的分子活动,为开发以信号传递系统为靶点的PTSD诊断和治疗方法开辟了道路。影响cAMP信号传递途径的基因非常多,引起该信号传递系统过度活化的基因也多种多样,可以推测与PTSD相关的基因突变也存在多样化的可能性。这些情况可能是迄今为止PTSD的致病基因没有固定在一个基因上的原因。”
原文:《科学新闻》
翻译:JST客观日本编辑部
【论文信息】
杂志:Molecular Psychiatry
论文:Fear memory regulation by the cAMP signaling pathway as an index of reexperiencing symptoms in posttraumatic stress disorder
DOI:10.1038/s41380-024-02453-4