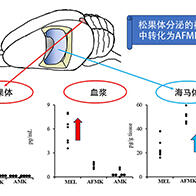
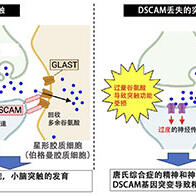
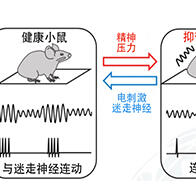
东京医科齿科大学研究生院医齿学综合研究科的横田隆德教授、永田哲也项目副教授和大谷木正贵(研究生)的研究团队宣布,利用独自开发的异源核酸成功实现了以往难以实现的淋巴细胞内源基因的高效控制。通过使用结合维生素E的异源核酸作为配体,可以高效控制靶淋巴细胞的α4β1整合素基因。经确认,给药后多发性硬化症小鼠等多种模型小鼠的病情均得到了改善。这一结果有望用来开发以前难以实现的与淋巴细胞相关的自身免疫性疾病等多种疾病的治疗药物。相关成果已经发布在国际科学期刊《Nature Communications》12月22日号上。
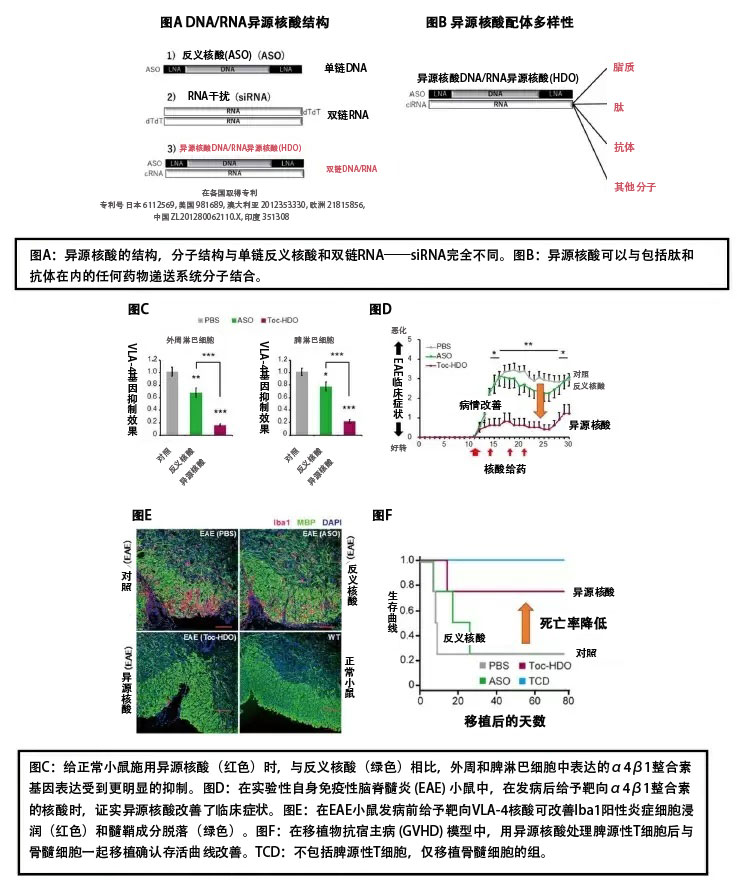
(供图:东京医科齿科大学)
核酸药物能都可对靶RNA进行选择性控制,目前全球已经批准15种核酸药物。其中就有作为脊髓性肌萎缩症等以往难以治疗疾病的治疗药物。另一方面,对于靶向淋巴细胞(B细胞、T细胞)进行治疗的自身免疫性疾病,由于淋巴细胞的药物吸收效率比较低,一直未能实用化。
研究团队此前开发出了分子结构和细胞内作用机理与反义核酸(ASO)和RNA干扰不同的DNA/RNA异源双链核酸(异源核酸),并确认高度有效。
此次进一步验证了异源核酸对淋巴细胞的有效性。首先以T细胞穿过血脑屏障时利用的粘附分子配体α4β1整合素(VLA-4)为靶标,设计了结合维生素E的异源核酸。对正常小鼠给药后确认,能以低于ASO的剂量持续且显著地抑制靶RNA。
对多发性硬化症模型小鼠(EAE:实验性自身免疫性脑脊髓炎)给药后确认,在T细胞和B细胞中均对RNA表达和蛋白质表达有高度抑制效果。发病前给药将发病时间延迟了10-15天,还能抑制T细胞的浸润和炎症,并确认到症状得到了改善。在被认为VLA-4与发病有关的移植物抗宿主病(GVHD)模型小鼠中也确认比ASO大幅降低了死亡率。
研究团队认为,与此前报告的ASO和异源核酸的吸收途径不同,可能存在异源核酸特有的吸收途径。
目前为进一步提高吸收效率,研究团队正与制药公司就异源核酸的结构进行联合研究。
原文:《科学新闻》
翻译编辑:JST客观日本编辑部