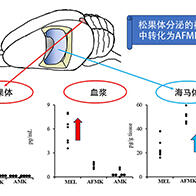
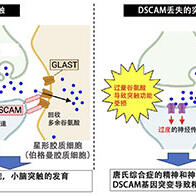
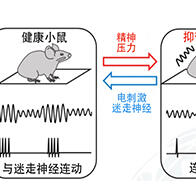
日本大阪大学等组成的研究团队日前宣布,明确了大多数胃癌的致病原因——幽门螺杆菌(Helicobacter Pylori)持续感染胃部的机制。研究发现幽门螺杆菌能够减少某种RNA(核糖核酸)的产生,从而使致癌因子的表达有所增加。该成果有望用于开发胃癌的诊断、预防及治疗方法。
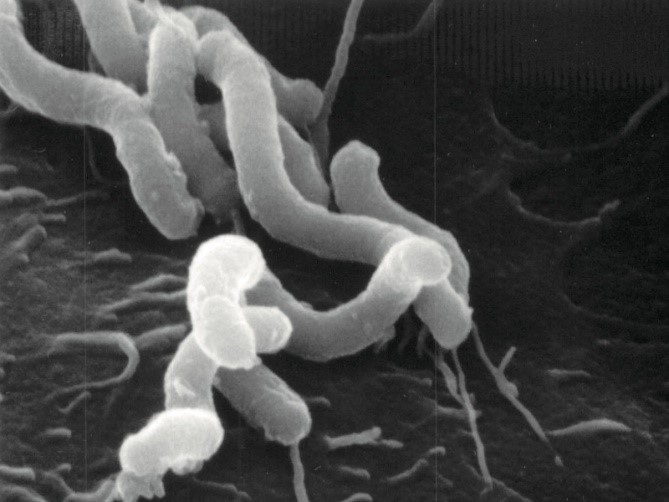
幽门螺杆菌显微镜照片(图片:大阪大学微生物病研究所)
儿童时期胃部如果感染幽门螺杆菌,几十年后会在病原性蛋白“CagA”的作用下引起萎缩性胃炎、胃溃疡和胃癌等消化系统疾病。全球有一半的人口都感染了幽门螺杆菌。但与那些会被身体立即消灭的病原细菌不同,幽门螺杆菌能长期持续感染胃部,而且一直不清楚与致癌因子之间的关系。此次,研究团队从感染了幽门螺杆菌的小鼠和长爪沙鼠的胃部提取出幽门螺杆菌,对基因组等进行了分析。
研究发现,胃部感染幽门螺杆菌后,负责调节“HPnc4160”(一种RNA)生成的基因组序列“T重复序列”会发生基因突变,长度变长。由此HPnc4160的数量出现减少,CagA等毒力因子出现增加,从而使幽门螺杆菌容易长期感染胃部。人类胃癌患者的幽门螺杆菌也是如此,菌株导致T重复序列出现长短变化,这种变化有利于感染持续。
HPnc4160是一种“小RNA”,它与相当于蛋白质设计图的“信使RNA”结合,帮助将遗传信息翻译给蛋白质,但其自身并不被翻译。
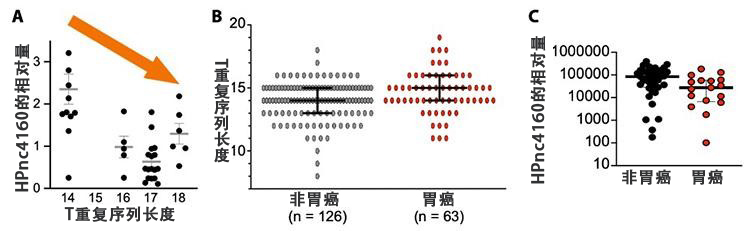
实验结果。(A)从长爪沙鼠胃部提取的幽门螺杆菌的T重复序列变长,HPnc4160减少;(B)胃癌患者的幽门螺杆菌的T重复序列比没有胃癌的人要长;(C)胃癌患者体内的HPnc4160较少(图片由大阪大学微生物病研究所提供)
幽门螺杆菌会使其外膜蛋白定植在胃粘膜上。一系列的研究表明,HPnc4160会调节这种蛋白质和CagA的表达。
本次研究的研究成员之一、大阪大学微生物病研究所副教授三室仁美(病原微生物学)介绍说:“此次明确了幽门螺杆菌持续发生感染的基本机制。作为基础研究意义重大。另外,有观点指出,幽门螺杆菌的阳性患者如果大量使用抗生素来根除细菌,会产生耐药菌增加的问题。因此,利用此次的成果还有望实现不消灭幽门螺杆菌,而是抑制幽门螺杆菌的病原性的新治疗方法。将来如果能通过调查T重复序列的长度和小RNA的表达确定治疗的优先次序的话,应该还有助于削减医疗费用。”
本次的研究团队由大阪大学、筑波大学、九州大学、大分大学、东京医科齿科大学和东京大学的研究人员组成。相关成果已于日本时间4月9日发表在英国科学期刊《Nature Communications》上。
【论文信息】
题目:A bacterial small RNA regulates the adaptation of Helicobacter pylori to the host environment
期刊:Nature Communications
URL:nature.com/articles/s41467-021-22317-7
日文:JST Science Portal 编辑部
中文:JST客观日本编辑部