本文根据冈山大学研究成果发布资料编译而成
日本冈山大学研究生院医齿药学综合研究科(医)的阿部康二教授和山下彻讲师,与东北大学研究生院医学系研究科的出泽真理教授组成的联合研究团队发现,为肌萎缩性侧索硬化症(俗称“渐冻症”,ALS)模型小鼠静脉注射来自人体骨髓的Muse细胞(多系分化持续应激细胞:Multilineage-differentiating Stress Enduring cells),可以抑制运动功能等的症状进一步恶化。
ALS是脑脊髓中的运动神经细胞持续减少,导致运动功能不断丧失的神经退行性难治之症,目前尚无根本性的治疗方法。研究团队此次确认,通过反复经静脉注射来自人体骨髓的Muse细胞,该细胞会移动到小鼠的脊髓(尤其是模型小鼠中受损严重的腰髓),分化为构成脊髓的细胞,能抑制运动神经细胞脱落和运动功能下降。
利用这项研究成果,有望针对遭受进行性运动功能丧失和呼吸肌麻痹痛苦的ALS患者开发新的治疗方法。
<背景>
肌萎缩性侧索硬化症(ALS)是一种神经退行性难治之症,多发生于中年以后,由于运动神经元选择性变性脱落,导致四肢肌肉无力并萎缩,出现构音障碍和吞咽困难,最终会因呼吸肌麻痹而引起呼吸衰竭,一般在发病3~5年后死亡。目前仍不清楚ALS的发病原因,主要使用谷氨酸酸拮抗剂利鲁唑和自由基清除药物依达拉奉治疗,尚不存在根本性的治疗药物。因此,迫切需要开发新的治疗方法。
另一方面,Muse细胞是一种体内存在的非肿瘤性多能干细胞,存在于骨髓、外周血和所有器官的缔结组织中。有报告显示,在心肌梗塞、脑梗塞、肾衰竭、肝损伤和皮肤损伤等多种损伤模型中,通过直接进行静脉注射,无需诱导分化,Muse细胞即可选择性地移动到受损部位并正常发挥作用,能自发分化为构成组织的细胞,从而修复组织,恢复其功能。
<研究成果>
为确定Muse细胞的给药途径,研究团队分别用静脉注射法和脊髓腔內注射法为ALS模型小鼠(G93A SOD1小鼠)注射了用绿色荧光蛋白(GFP)标记的人骨髓Muse细胞,7天后进行了调查。静脉注射组在颈髓和腰髓的软膜及白质中检测出大量Muse细胞,而脊髓腔內注射组仅在脊髓中发现微量的GFP标记Muse细胞。GFP标记Muse细胞的存活总数在静脉注射组高于脊髓腔內注射组,且再现性良好,因此研究团队选择静脉注射作为合适的给药途径。
另外,为确认仅进行静脉注射,Muse细胞是否能真正到达脊髓,研究团队利用检测灵敏度比较高的纳米灯笼实施了Ex vivo成像实验。为对照组静脉注射用纳米灯笼标记的人骨髓间充质干细胞(Mesenchymal stem cell:MSC)后,在肺部检测到大量聚集,在大腿骨中检测到微量聚集,但在脊髓中未检测到信号。而Muse细胞在脊髓中明确检测到信号,此外在肺部和大腿骨中也检测到信号。以上结果表明,人Muse细胞可通过静脉注射移动到ALS小鼠的脊髓中(图A)。
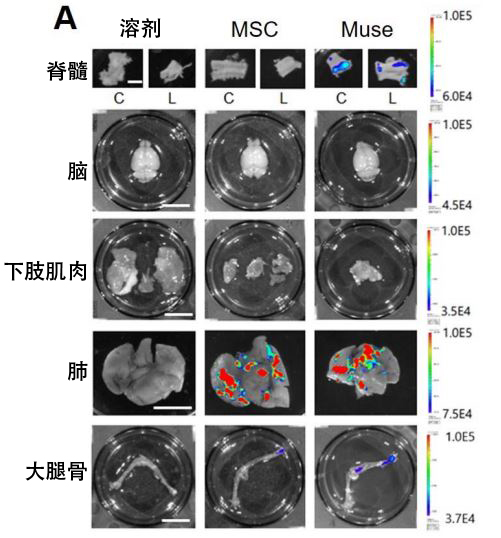
图A:在利用纳米灯笼进行Ex vivo成像的实验中,仅在Muse细胞注射组的脊髓中检测出纳米灯笼信号。
接下来,为确认Muse细胞的治疗效果,研究团队为出生56天后的ALS小鼠每周静脉注射一次人Muse细胞(5万细胞/次),连续注射10周。对照组以同样的频率注射溶剂和人MSC(5万细胞/次)。然后实施了转棒行走测试(Rotor-rod test,全身运动功能)、挂线测试(Hanging Wire Test,四肢肌肉力量)和下肢肌肉力量测试等多种运动功能评估测试,确认与溶剂注射组和MSC组相比,Muse细胞注射组的运动功能出现改善的倾向,其中与溶剂注射组之间的差异尤其明显。在ALS小鼠的腰髓(模型小鼠中损伤尤其严重的部位)中,脊髓软膜及其下方的白质和脊髓前角中观察到了GFP标记的Muse细胞,其中85.7%的细胞表达星形胶质细胞的标志物GFAP(图B、C)。另外,在ALS小鼠脊髓前角中的残余运动神经元数量、接受神经投射的突触数量,以及胫前肌肌纤维的大小方面,Muse细胞注射组也比溶剂注射组有明显的改善。
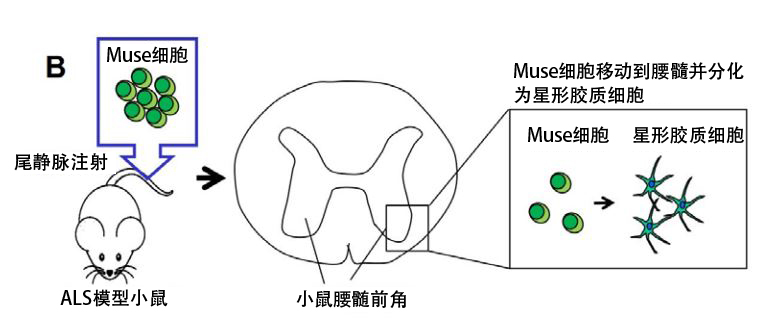
图B:经尾静脉注射的Muse细胞到达腰髓,主要分化成星形胶质细胞。
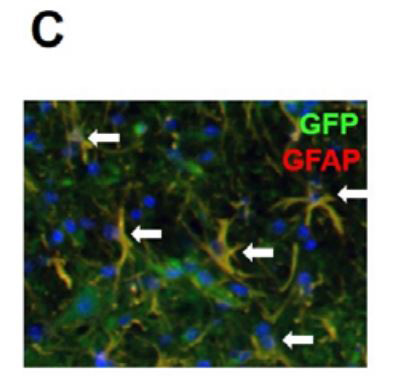
图C:用GFP标记的Muse细胞在腰髓内表达星形胶质细胞标志物GFAP。
论文信息
题目:Therapeutic benefit of Muse cells in a mouse model of amyotrophic lateral sclerosis
期刊:Scientific Reports
DOI:10.1038/s41598-020-74216-4
编译:JST客观日本编辑部