日本庆应义塾大学理工学部的古川良明副教授、德田荣一助教(研究当时;现为日本大学药学部专任讲师)及研究生院理工学研究科的安斋树等人,与同大学药学部的三泽日出巳教授和自然科学研究机构分子科学研究所的秋山修志教授等联合研究,就肌萎缩性侧索硬化症(ALS)发病关联的铜/锌离子结合蛋白SOD1,提出了引起其三级结构异常的新机制。SOD1的编码基因发生突变后,三级结构异常的SOD1会在运动神经元中积累,从而引发ALS。
虽然尚不清楚SOD1结构发生异常的原因,但本次发现氧化的SOD1在铜/锌离子解离后,会转换成有毒异常结构。据报告,很多ALS患者都会出现氧化应激加剧和金属离子动态异常的现象,因此本研究对探讨与SOD1关联的ALS发病机理至关重要。
铜锌超氧化物歧化酶(SOD1)是铜离子和锌离子络合金属蛋白,起着将高反应性活性氧——超氧化物转换为氧分子和过氧化氢的重要作用。已发现在部分ALS患者体内编码SOD1的基因发生了突变,错误折叠的SOD1会在脊髓的运动神经中积累。另外,SOD1编码基因未突变的原因不明散发性ALS患者脑脊液中,也检测出了高毒性的错误折叠SOD1。也就是说,SOD1的三级结构异常(错误折叠)可能与ALS发病有关,虽然一直不清楚其触发因素。
研究团队从ALS患者的脊髓及周边脑脊液中,氧化应激标志物数值畸高,很多生物分子都易被氧化的情况入手,考虑到SOD1产生的过氧化氢是强氧化剂,研究团队认为SOD1可能伴着氧化而发生了错误折叠。
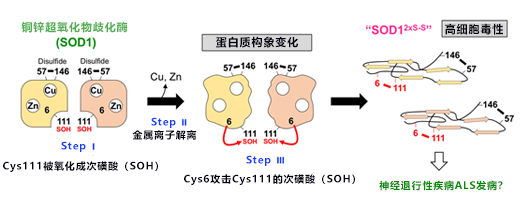
图1:本次研究提出的SOD1错误折叠新机制
众所周知,在构成蛋白质的氨基酸中,半胱氨酸(Cys)是最容易被氧化的。SOD1含有4个半胱氨酸。在正常折叠的SOD1中,其中Cys57和Cys146氧化形成“二硫(S-S)键”, 保持立体结构稳定;另外2个半胱氨酸(Cys6和Cys111)一般不会被氧化。但本研究发现,ALS患者的SOD1在产生的过氧化氢作用下,Cys111被氧化成了次磺酸状态(图1)。
另外,络合的铜离子和锌离子解离后,蛋白质结构发生很大变化。通常位于较远位置的Cys6会攻击Cys111转化的次磺酸,从而在Cys6与Cys111之间也形成S-S键(图1)。
也就是说,随着氧化应激的加大和铜、锌离子解离,会形成含有2个S-S键的异常结构SOD1(SOD12xS-S)。该SOD12xS-S容易聚集成不溶性沉淀,当将其添加到运动神经元样培养模式细胞NSC-34中之后显示出了毒性,表现出了正常SOD1所不具备的性质。
论文信息
题目:Oxidative misfolding of Cu/Zn-superoxide dismutase triggered by non-canonical intramolecular disulfide formation
期刊:《Free Radical Biology and Medicine》
DOI:10.1016/j.freeradbiomed.2019.12.017
文:JST客观日本编辑部编译