日本东京医科齿科大学与九州大学通过联合研究发现,CKD(慢性肾脏病)的各种因子如尿毒症毒素等,会造成活化蛋白激酶(AMPK)对负责细胞能量稳态的AMP(Adenosine monophosphate,腺苷一磷酸)出现感知障碍,从而导致肾脏陷入能量衰竭的状态。相关研究成果于2018年11月16日发布在国际科学杂志《Kidney International》的在线版上。
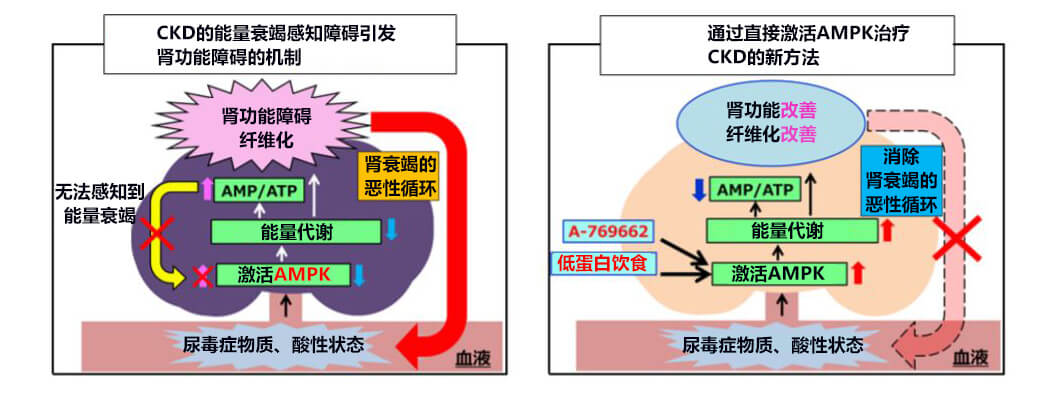
正常情况下,AMPK会察觉到AMP上升造成的能量衰竭并改善能量状态,但患慢性肾病时,受尿毒症物质等的影响,AMPK对AMP的易感性降低,导致肾功能障碍持续恶化。研究小组为评估患慢性肾病的肾脏能量状态和尿毒症毒素等代谢物的积累情况,对CDK模型小鼠的肾脏组织进行代谢学分析,综合分析了代谢物的种类和浓度。
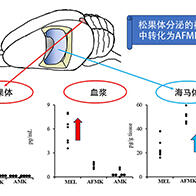
ATP(Adenosine triphosphate,三磷酸腺苷)是生物体内的能量来源,通过释放能量形成AMP。研究小组确认,在慢性肾病患者的肾脏中,AMP/ATP的比例升高,这意味着细胞内的能量减少,能量状态与正常的肾脏相比出现恶化。
研究小组着眼于作为能量传感器发挥着重要作用的AMPK,如果细胞内的能量减少,也就是AMP/ATP比升高,AMPK就会被激活,从而促进ATP的产生,改善能量状态。但研究小组发现,在慢性肾脏病患者的肾脏中,即使AMP/ATP比升高、能量状态恶化,但由于肾病造成尿毒症毒素积累以及体内环境酸性化等,出现了AMPK未被激活的“能量衰竭感知障碍”。
对此,研究小组向CKD模型小鼠投用了无需经由AMP/ATP感知机构、能直接激活AMPK的药剂A-769662,发现可以激活肾脏的AMPK,阻止肾功能障碍进一步恶化。这表示,此药有望成为根据“能量衰竭感知障碍”治疗CKD的新方法。
另外,低蛋白饮食一直被认为是重度慢性肾脏病的有效饮食疗法,不过此前并不清楚其分子学机制。此次研究小组发现,低蛋白饮食与A-769662一样,都是不经由AMP/ATP就能强烈激活AMPK,从而抑制慢性肾病引起的肾功能障碍和纤维化。
利用此次的研究成果,今后有望实现能取代低蛋白疗法的慢性肾脏病新疗法。
文 客观日本编辑部
日文发布全文 [PDF]