日本东京大学的研发小组利用基于多能干细胞嵌合体形成能力的“囊胚互补法”,在血管内皮细胞和血液细胞缺损的小鼠体内,成功培养出了源自小鼠胚胎干细胞(ES细胞)及诱导性多能干细胞(iPS细胞)的血管内皮细胞和血液细胞。
通常,血管内皮细胞和血液细胞缺损的小鼠在发育初期的胎儿期就会死亡,但利用囊胚互补法向小鼠受精卵注入小鼠ES细胞或iPS细胞培养的嵌合体小鼠,其体内缺损的血管内皮细胞及血液细胞被替换成源自ES细胞或iPS细胞的内皮细胞和血液细胞,不会出现肿瘤等异常,能正常发育为成体。
研究小组此前一直致力于在动物体内培养源自多能干细胞的脏器,结合此次的研究成果,除目标脏器外,还能同时利用多能干细胞培养脏器内的血管内皮细胞和血液细胞。作为不容易在动物体内发生排异反应的移植用脏器培养方法,这项研究成果有望为再生医疗做出巨大贡献。
相关论文于2018年9月20日发表在科学杂志《干细胞报告》(Stem Cell Reports)的在线版。
<研究内容>
东京大学医科学研究所特聘教授中内启光等人组成的研发小组,此前利用基于多能干细胞嵌合体形成能力的“囊胚互补法”,在胰脏缺损的小鼠和大鼠体内,成功培养了源自异种大鼠或小鼠多能干细胞的胰脏,并确认,利用囊胚互补法在动物体内的脏器所含的血管和神经等支持组织为嵌合体状态(混有异种动物细胞的状态)。
进行脏器移植时,作为供体的移植脏器内存在的MHC不相容血管内皮细胞会成为排异反应的靶细胞。另外,供体脏器中残存的血液细胞会攻击受体的脏器,发生移植物抗宿主反应(GVHD)。因此,要想培养不容易发生排异反应和GVHD的移植脏器,除脏器外,还需要同时利用多能干细胞培养脏器内的血管内皮细胞和血液细胞。
在本项研究中,为培养源自多能干细胞的血管内皮细胞和血液细胞,研发小组利用血管内皮细胞和血液细胞缺损(FIK-1基因缺损)的小鼠受精卵进行了囊胚互补(图1)。
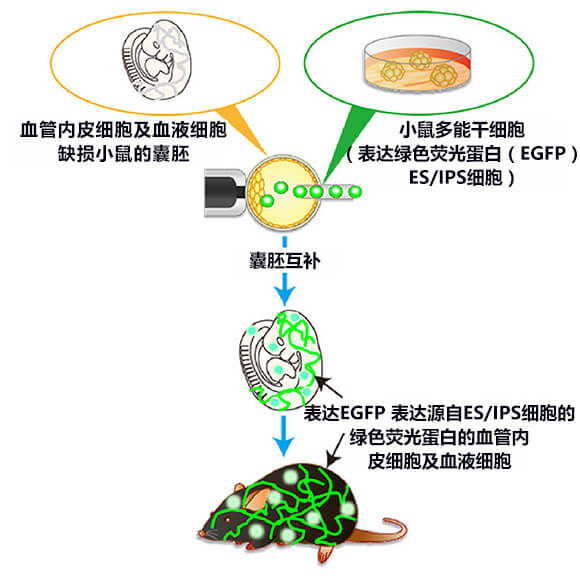
图1:研究概要图解
血管内皮细胞和血液细胞缺损的小鼠在发育初期的胎儿期就会死亡,研发小组向这类小鼠的囊胚注入表达绿色荧光蛋白FPFG的小鼠多能干细胞(ES细胞或iPS细胞),在血管内皮细胞和血液细胞缺损的嵌合体小鼠体内培养源自小鼠多能干细胞、表达FPFG的血管内皮细胞和血液细胞(囊胚互补)。小鼠身上的绿色线表示源自表达FPFG的小鼠多能干细胞的血管内皮细胞和血液细胞。
通常,血管内皮细胞和血液细胞缺损的小鼠在发育初期的胎儿期就会死亡,但利用囊胚互补法为这类小鼠的受精卵注入多能干细胞培养的嵌合体小鼠,未出现肿瘤等异常,顺利发育为成体,研发小组成功培养了源自小鼠多能干细胞的血管内皮细胞和血液细胞(图2)。
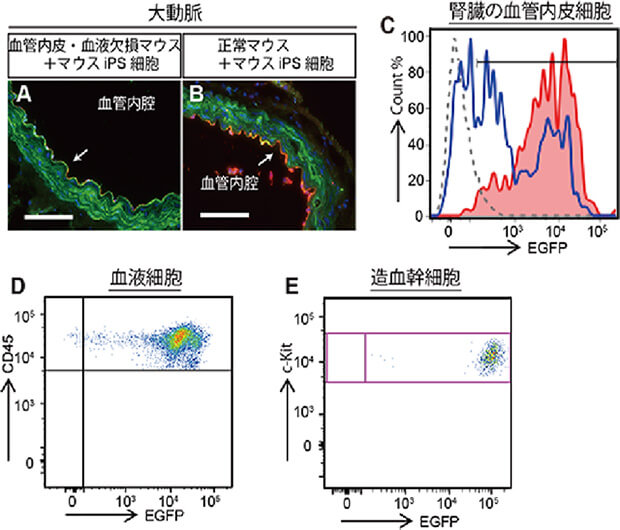
图2:利用小鼠多能干细胞在发育为成体的血管内皮细胞和血液细胞缺损小鼠体内培养的血管内皮细胞和血液细胞
(A、B)为大动脉的组织切片图像,血管内腔侧为血管内皮细胞(箭头)。血管内皮细胞呈红色荧光,源自小鼠多能干细胞的细胞呈绿色荧光。(A)面向血管内皮细胞和血液细胞缺损小鼠培养的血管内皮细胞源自小鼠iPS细胞,(B)在向正常小鼠囊胚中注入iPS细胞培养的嵌合体小鼠中,源自小鼠iPS细胞的血管内皮细胞只有一部分。在(A、B)中,白线长度表示100微米。(C)为肾脏的血管内皮细胞嵌合体。向血管内皮细胞和血液细胞缺损的小鼠囊胚注入iPS细胞培养的嵌合体小鼠,其血管内皮细胞源自表达FPFG的小鼠iPS细胞(红线)。在向正常小鼠囊胚注入iPS细胞培养的嵌合体小鼠中,源自表达FPFG的小鼠iPS细胞的血管内皮细胞只有一部分(蓝线)。虚线表示未注入iPS细胞的正常小鼠。在血管内皮细胞和血液细胞缺损小鼠体内培养的(D)血液中的血液细胞(CD45阳性细胞)和(E)骨髄中的造血干细胞(c-Kit阳性/Sca-1阳性/Lineage阴性细胞),源自FPFG阳性的小鼠多能干细胞。
研发小组的目标是在其他动物体内培养人类的脏器用于移植治疗,结合此次的成果,不仅是脏器,还能同时利用多能干细胞培养脏器内的血管内皮细胞和血液细胞,由此便可实现采用囊胚互补法的不容易发生排异反应的移植用脏器培养方法,有望为脏器再生和再生脏器的移植治疗做出巨大贡献。
文 客观日本编辑部
日文发布全文 [网址]