京都大学等的研究团队发表成果称,利用从诱导多能干细胞(iPS细胞)制备的肾脏前体细胞移植到慢性肾脏病(CKD)小鼠体内后,成功抑制了小鼠的肾功能衰退。研究团队表示将在确认安全性的基础上,力争数年内启动临床试验。据估算,日本国内约有2000万CKD患者,病情进展至终末期肾衰竭阶段时需要接受人工透析或肾脏移植。
京都大学iPS细胞研究所的长船健二教授、荒冈利和讲师等人的研究团队,此前已将利用iPS细胞制备的肾前体细胞(肾单位前体细胞)移植至再现急性肾损伤状态的小鼠体内,确认获得了治疗效果。此后,团队继续开展推动CKD治疗的研究,并成功构建了CKD模型小鼠。这种小鼠在1~6个月内,会逐渐出现肾功能衰退的纤维化症状。
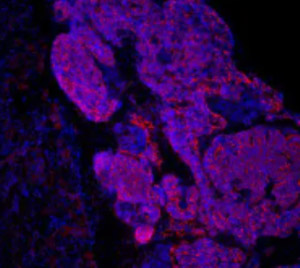
移植至CKD小鼠肾脏中的iPS细胞来源肾前体细胞(粉色发光部分)(供图:京都大学iPS细胞研究所)
然而,要将从iPS细胞制备的肾脏前体细胞应用于人类治疗,还需高效扩增肾前体细胞,以达到每人约10亿个的细胞量。大量制备具有预期治疗效果的高质量肾前体细胞,一直是个课题。
研究团队此次开发出一种在带有近100个孔的培养板中,每孔置入约2万个细胞团块,再加入特殊培养液(CFY培养液)以形成细胞聚集体的新方法。这种方法能将细胞扩增至原有数量的100倍以上,且生成的细胞质量也很高。
长船教授等人基于这些成果,将大量肾前体细胞移植到CKD小鼠的肾包膜(覆盖肾脏的膜)下。结果发现,移植3天后,血尿素氮(BUN)和血清肌酐值等“数值越高肾功能衰退越严重”指标的上升趋势得到了抑制。此外,纤维化状态也未进一步恶化。
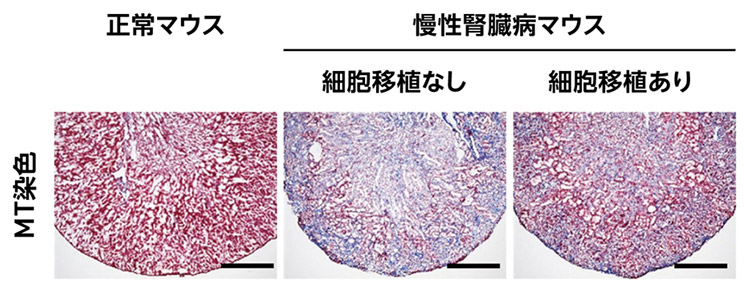
实验小鼠的肾脏。图片中央的iPS细胞来源肾前体细胞对应的“未进行细胞移植”小鼠的肾脏组织可见纤维化进一步发展。而“进行细胞移植”小鼠的肾脏组织可见已接近正常小鼠状态(供图:京都大学iPS细胞研究所)
对于此实验成果,研究团队认为,移植细胞分泌的蛋白质(VEGF-A)促进了血管新生,从而减轻了肾脏损伤。
研究团队介绍说,CKD是一种表现为肾功能慢性持续衰退的状态,且难以完全治愈,若病情恶化则会发展为不接受人工透析或肾脏移植就难以维持生命的终末期肾衰竭。因此,利用iPS细胞等技术的再生医疗的实现备受期待。相关研究论文已发表在国际科学期刊《Science Translational Medicine》的4月2日刊上。
利用iPS细胞的再生医疗目前在多个医学领域正推进面向实用化的研究。京都大学iPS细胞研究所名誉所长兼教授的山中伸弥于2007年开发出人类iPS细胞的生成技术,一举受到全球关注。该技术的特长是能够分化为多种细胞,主要目标是再生因疾病或受伤而丧失功能的组织和器官。
自2014年国立研究开发法人理化学研究所等机构首次向患有视网膜疾病“老年性黄斑变性”的患者进行移植以来,日本国内除iPS细胞研究所外,大阪大学、庆应义塾大学等机构也正在对帕金森病、心力衰竭、脊髓损伤等多种疾病的治疗领域推进临床试验及临床应用研究。
其中,京都大学iPS细胞研究所2025年4月17日公布了将利用iPS细胞制备的神经细胞(iPS来源多巴胺神经前体细胞)移植到帕金森病患者大脑的临床试验结果。据介绍6名患者中有4人的运动功能得到改善,显示出了该疗法的效果。
原文:JST Science Portal 编辑部
翻译:JST客观日本编辑部
【相关链接】
京都大学iPS细胞研究所
京都大学iPS细胞研究所新闻稿 在小鼠中确认细胞疗法对慢性肾脏病(CKD)的疗效——目标数年内启动临床试验
京都大学iPS细胞研究所新闻稿 “使用iPS细胞来源多巴胺神经前体细胞的帕金森病治疗相关医生主导治疗试验”提示安全性和有效性
【论文信息】
期刊:Science Translational Medicine
论文:Human iPSC-derived nephron progenitor cells treat acute kidney injury and chronic kidney disease in mouse models
DOI:10.1126/scitranslmed.adt5553