日本庆应义塾大学医学部的市原元气助教(研究当时)、佐野元昭副教授、该大学体育医学综合中心的胜俣良纪专任讲师和京都大学研究生院医学研究科的杉浦悠毅特定副教授的联合研究团队发表研究成果称,发现了一种着眼于心肌梗塞的代谢变化的新治疗方法。研究团队利用疾病模型小鼠,通过“利用代谢分子的监测方法”详细观察了心肌缺血再灌注损伤的阶段性进展过程,发现该疾病是由保护心肌的重要因子——谷胱甘肽(一种还原物质,多肽的一种)通过载体“MRP1”被释放到细胞外而引起的。研究还证实,通过干预增强活性氧清除的代谢路径,可以减少心肌缺血再灌注损伤后的心肌损伤。该成果有望推动心肌梗塞后的康复。相关成果已刊登在《Circulation Research》杂志10月11日号上。
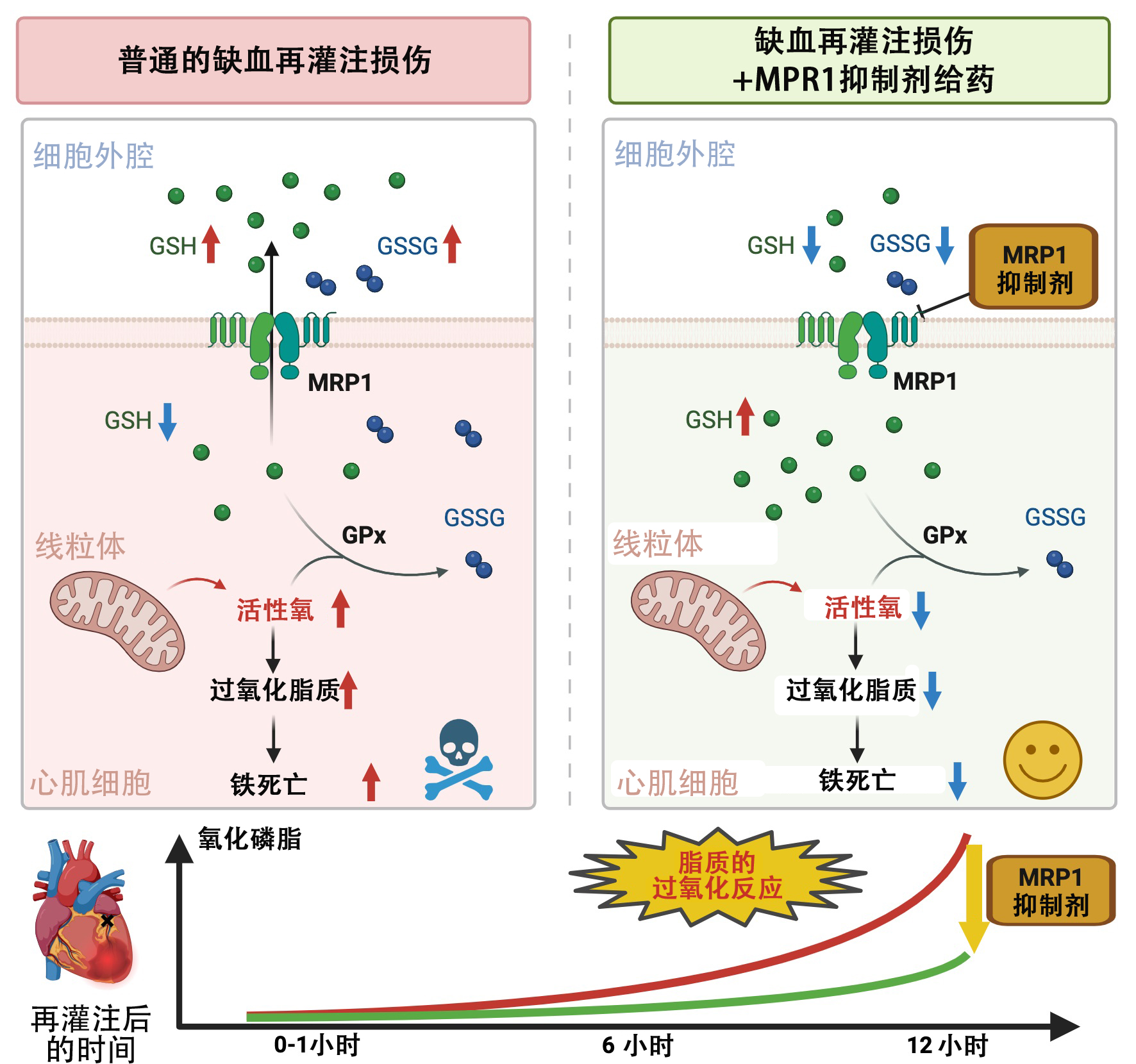
心肌缺血再灌注损伤的进展机制和MPR1抑制剂给药的效果。(供图:庆应义塾大学医学部)
GSH:还原型谷胱甘肽
GSSG:氧化型谷胱甘肽
GPx:谷胱甘肽过氧化物酶
心肌梗塞(缺血性心脏病)是全球范围内排名靠前的死亡疾病,近年来随着治疗技术的提高,抢救成功率已显着提升。另一方面,由于心肌梗塞引起的缺血再灌注损伤,心脏泵血功能降低,许多患者在抢救后会出现心力衰竭,而目前尚未确立针对此的治疗方法。缺血性再灌注损伤是由于缺血心肌在血流恢复后迅速再氧化,产生大量活性氧,使得细胞内各种蛋白质变性而引起的。
为此,研究团队利用大鼠心脏再现了缺血再灌注损伤,并在活体状态下持续分析了这一过程中产生的代谢物质变化。研究人员采用将筒状半透膜植入心壁,连续收集并测量透过半透膜的心肌间质代谢物的方法(微透析法)。传统方法通过收集同一损伤后的心肌细胞并分析代谢物等来寻找目标分子,但无法跟踪随时间快速变化的心肌代谢状态。
结果,研究人员成功地在缺血前、缺血中和再灌注后的3个阶段,分别连续收集到了同一活体心肌间质中的代谢物。研究人员还发现,心肌保护的关键因子,同时也是强力还原性物质的“谷胱甘肽”在缺血和再灌注阶段会被释放到细胞外,从而变得无法清除细胞内的活性氧类。
细胞内谷胱甘肽的枯竭会使活性氧类增加,导致脂质过氧化和因细胞膜脂质过度氧化而引发的细胞死亡(铁死亡)。
此外,研究人员还发现这种细胞外释放主要由一种被称为MRP1的特殊载体介导。
于是,研究人员使用药物抑制了MRP1的功能,结果发现谷胱甘肽保留在细胞内,不仅活性氧被清除,氧化脂质也减少了,由此可知谷胱甘肽可以支持心肌细胞的存活。
此外,研究还证实,这种以铁死亡为靶向的治疗法即使在缺血再灌注后数小时开始也具有一定的效果。
针对心肌梗塞发病6小时后出现的氧化脂质增加的情况,有望通过治疗药物延缓给药实现有效的治疗。
胜俣专任讲师介绍说,在这项研究中,通过采用新技术“利用代谢分子的监测”方法,成功地明确了由心肌梗塞引发的有害活性氧清除机能逐渐下降的机理。利用这一发现,我们揭示了对抗氧化应激的重要防御物质——谷胱甘肽在缺血和再灌流时会泄漏到细胞外的现象。我们期望这一发现能为开发新的心肌梗塞治疗方法开辟道路。
原文:《科学新闻》
翻译:JST客观日本编辑部
【论文信息】
杂志:Circulation Research
论文:MRP1-dependent Extracellular Release of Glutathione Induces Cardiomyocyte Ferroptosis After Ischemia-Reperfusion
DOI:10.1161/CIRCRESAHA.123.323517