肌萎缩性侧索硬化症(Amyotrophic lateral sclerosis:ALS,俗称"渐冻症“)患者意识和感官清醒,但身体完全无法运动,是目前尚无法彻底治愈的最残酷的难治性疾病之一。由于不清楚ALS受损的“运动神经元”细胞是何时及如何开始丧失功能的,阻碍了治疗方法的开发。
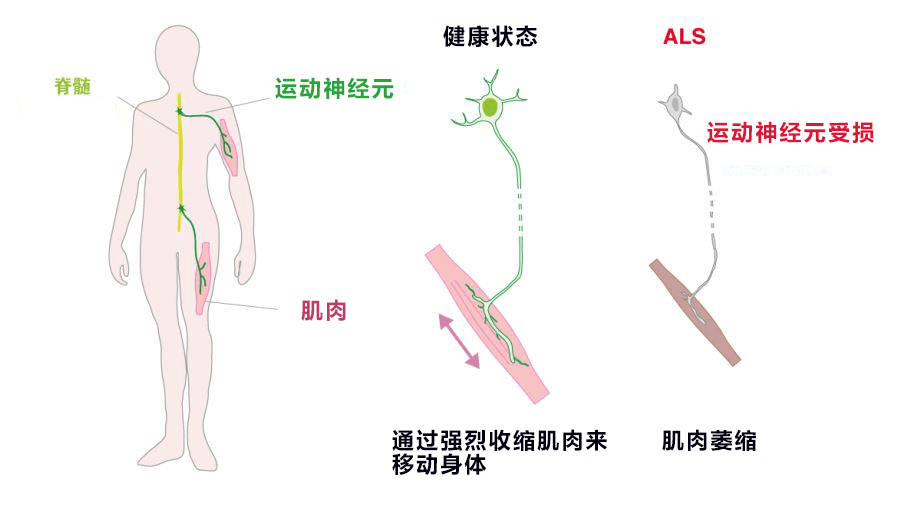
图1:在ALS中,运动神经元受损,肌肉萎缩。
为解决这个问题,研究团队开发出了利用光操作TDP-43蛋白的技术,全球首次通过光照射成功再现了ALS存在的各种运动神经元异常现象。
东京医科大学的浅川和秀副教授等人修改了会在ALS的运动神经元中形成团块的TDP-43,使其吸收蓝光便能形成团块,由此开发出了通过照射光自由调节团块形成的技术。研究发现,一旦照射光后,即使在TDP-43形成团块之前停止照射,运动神经元也会出现异常。这表明,TDP-43损伤运动神经元的时间早于之前的预期。在形成团块之前防止TDP-43聚集有望成为有效的ALS治疗法。
研究背景
ALS是一种意识和感官始终清醒,但全身肌肉逐渐萎缩的难治性神经系统疾病。每10万人中大约有2人罹患此病,在日本大约有9,200名病人。发病后平均2~3年就会死亡,是一种被称为“顽症中的顽症”的残酷疾病。ALS是收缩肌肉的神经细胞“运动神经元”发生变性引起的(图1)。90%以上的ALS属于没有家族病史的散发型,ALS并不是由单个基因突变引起的,所以迟迟没有查清发病机制。14年前的研究发现,散发性ALS的运动神经元中所形成团块的主要成分是TDP-43蛋白质。但研究位于身体深处的运动神经元的TDP-43非常困难,多以始终未能验证TDP-43的团块与运动神经元变性之间的因果关系。
研究成果
此次,研究团队开发了通过照射光调节团块形成的修饰型人TDP-43,并在模式生物斑马鱼体内成功再现了与ALS状态非常相似的运动神经元异常。由此发现,TDP-43团块是通过两步形成的,即蛋白质聚集引起的“从细胞核向细胞质移动”,以及“在细胞质中形成团块”(图2)。另外还发现,即使仅调节光的照射量诱导TDP-43“从细胞核向细胞质移动”,也会引起运动神经元萎缩,导致其与肌肉的结合减弱。长时间持续照射光后,还出现了游动变得困难的鱼。
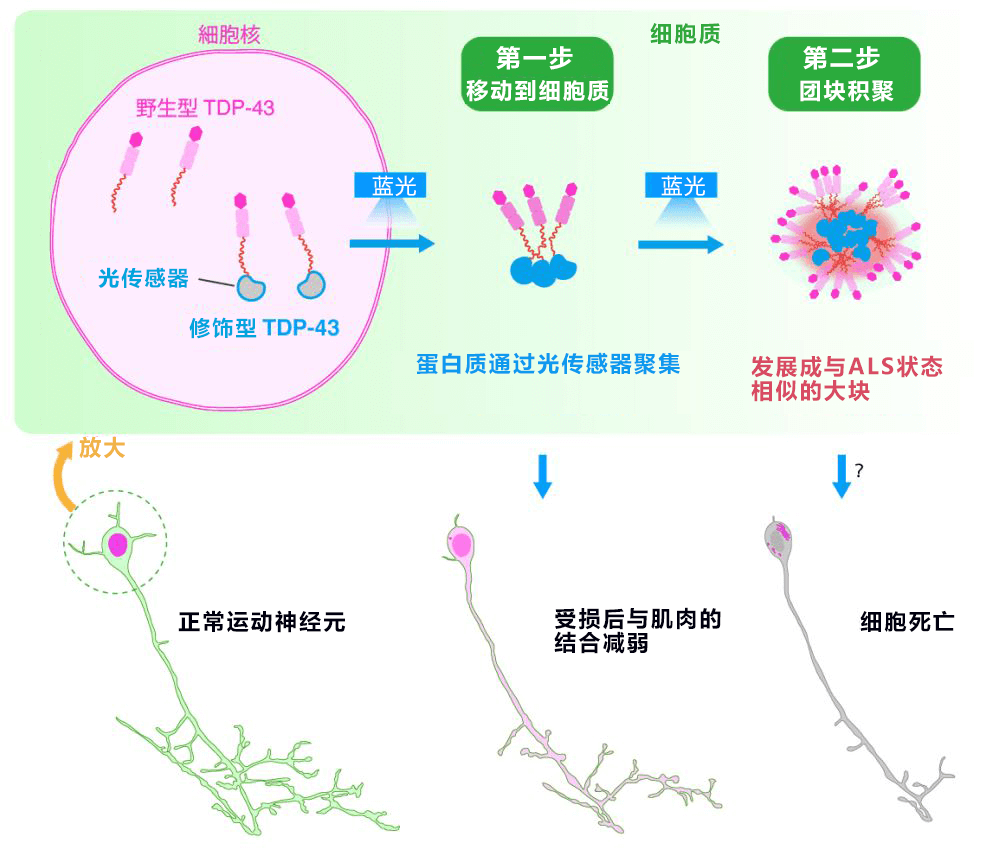
图2:随着TDP-43向细胞质移动,运动神经元受损,与肌肉的结合减弱。
运动神经元是形状复杂的大细胞,人类和小鼠等大型实验模型动物很难获得细胞的整体图像,这也成为研究ALS的障碍。而体型小巧、近乎透明的斑马鱼很适合用来观察运动神经元。此次,研究团队利用过去10年来自主开发的斑马鱼操作和观察技术(图3),使“利用光远程操作位于体内深处的运动神经元中的TDP-43”,以及“长时间详细观察运动神经元整体由此发生的变化”成为可能,最终获得了此次的研究成果。
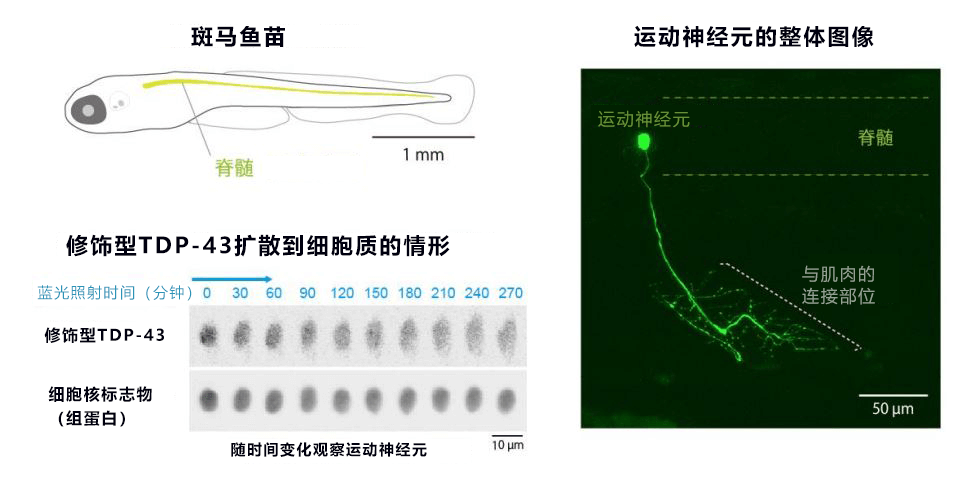
图3:可以观察活体动物运动神经元的整体图像以及其中活动的TDP-43。
未来展望
本研究全球首次发现,从TDP-43开始形成团块之时起,运动神经元就开始丧失功能了。因此,在形成团块之前防止TDP-43聚集有可能将是治疗ALS的有效方法。
论文信息
题目:Optogenetic modulation of TDP-43 oligomerization accelerates ALS-related pathologies in the spinal motor neurons
期刊:《Nature Communications》
DOI:10.1038/s41467-020-14815-x
文:JST客观日本编辑部编译