东京大学定量生命科学研究所的清水谦次特任助教和冈崎拓教授等人组成的研究团队,详细调查了PD-1对T细胞基因表达的影响。调查发现,有些基因的表达增加会受到PD-1抑制,而有些则不会。研究团队同时还查清了这些基因的特征。
目前,PD-1抑制剂抗体药作为癌症治疗药物应用于很多患者身上。但根据癌症类型和个体的不同,其效果也大相径庭。此次的研究成果有望应用于改良使用PD-1抑制剂抗体药的癌症免疫疗法及开发新的免疫调控疗法。
【研究背景】
在保护人体免受病原体和癌细胞侵害的免疫系统中,T细胞同时担当指挥和执行者的角色,通过识别各T细胞的特异性抗原而被激活。T细胞被激活后,各种基因表达会相应发生变化,表现出存活、增殖、分化及产生细胞因子等应答。
因通过解除免疫抑制开发出了癌症免疫疗法,2018年的诺贝尔生理学或医学奖被颁发给本庶佑博士和詹姆斯·艾利森博士。通过两位博士的研究确认,虽然在未治疗状态下已经诱导了对癌细胞的免疫反应,但效果被PD-1及CTLA-4等抑制性免疫辅助受体(即免疫检查点分子)削弱。可以通过阻碍抑制性免疫辅助受体的功能可以激活癌细胞特异性T细胞,从而达到治疗癌症的目的。冈崎教授2008年之前一直在京都大学的本庶研究室从事研究,查清了PD-1抑制的分子机制等,确认PD-1是一类能抑制对自身的不适当免疫反应和癌症免疫反应的抑制性免疫辅助受体。
此前就知道PD-1会抑制T细胞的活性化,但不清楚其究竟是如何改变T细胞的基因表达的。在T细胞上表达的抗原受体(T细胞受体,TCR)识别抗原后,TCR会被磷酸化,并向下游传递信号。
由于PD-1是通过削弱TCR的磷酸化抑制T细胞被激活,此前一直认为PD-1会以相同的方式抑制因T细胞被激活而引起的所有基因表达变化。但PD-1发挥作用时,T细胞会暂时或长期陷入功能失调状态等,即PD-1会使T细胞的功能发生质的变化。如以相同方式抑制所有基因表达变化的话则无法解释为什么T细胞会发生质变,因此PD-1是如何调控T细胞活性化的始终是个谜。
【研究内容】
此次,研究团队首先在PD-1工作和不工作的条件下分别对T细胞进行抗原刺激,全面调查了各基因表达量。调查发现,对T细胞进行抗原刺激时表达量增加的基因既包括容易被PD-1抑制的基因也有不容易被抑制的基因(图1)。
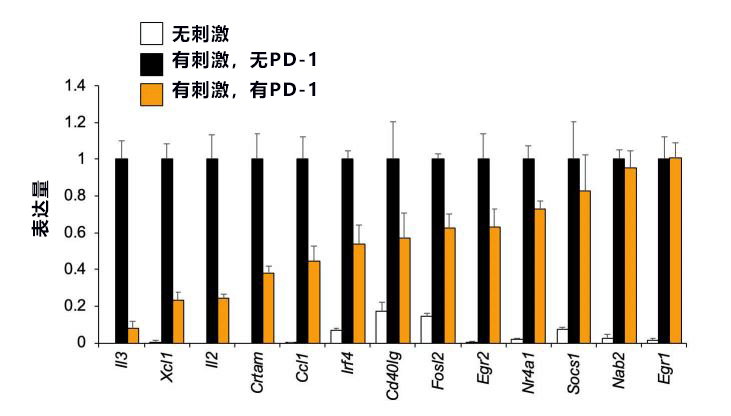
图1:随着T细胞被激活表达增加的基因包括容易被PD-1抑制的基因和不容易被抑制的基因
接下来,研究团队改变了刺激T细胞的抗原的量并进行解析发现,表达增加所需的抗原量因基因而异。因此,计算了诱导各基因表达量增加至最大表达增加量一半时的抗原浓度(半最大效应浓度,EC50)。计算发现,不同基因的EC50值最大相差482倍。另外还发现,PD-1的抑制效果与EC50呈正相关(图2)。也就是说,越是需要强烈刺激才能增加表达量的基因,越容易被PD-1抑制。
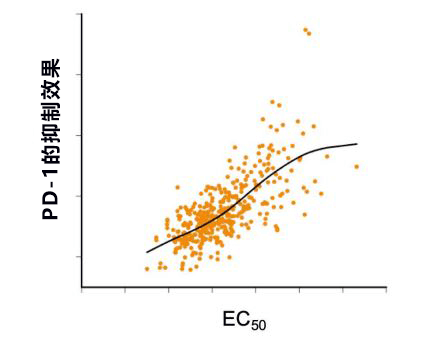
图2:EC50的值越高的基因,越容易被PD-1抑制
研究团队调查基因的启动子序列特征与PD-1的抑制效果间的关系时发现,容易被PD-1抑制表达增加的基因,启动子序列的CpG频率较低,浓缩了几种比较有特点的转录因子结合基序。
研究认为,各基因的EC50由CpG的频率与转录因子结合基序的组合等决定,PD-1抑制各基因表达的增加与EC50的值相对应。
最后,研究团队调查了表达增加容易被PD-1抑制的基因的功能性特征。调查发现,PD-1会选择性地抑制细胞因子和CD40L等在T细胞实际工作时发挥作用的基因表达。另一方面,PD-1对与转录、细胞凋亡和信号转导等有关的基因表达则几乎没有影响(图3)。
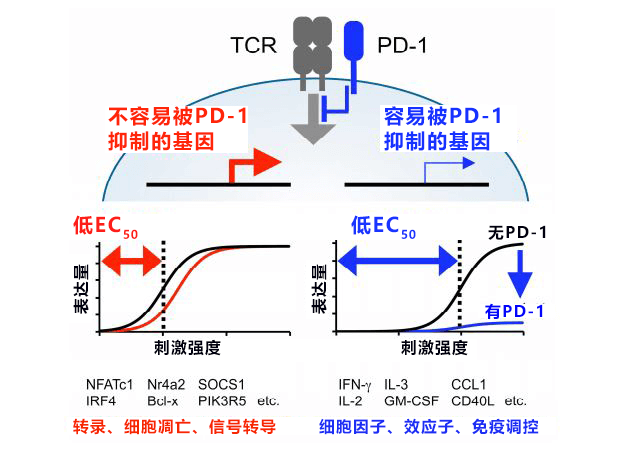
图3:PD-1的T细胞活性化调控机制
以上结果表明,PD-1并不是单纯削弱T细胞的活性化程度,而是通过选择性抑制特定基因,使T细胞发生质的变化。实验证明,被PD-1抑制活性化的T细胞与单纯地被少量抗原微弱刺激的T细胞有着质的区别。希望今后能查明PD-1在抑制自身免疫和癌症免疫方面具有这种特性的意义。
【社会意义】
PD-1抑制剂抗体药的治疗效果因癌症类型和个体而大不相同。癌症特异性T细胞的功能被PD-1抑制越强烈,认为PD-1抑制剂抗体药越有效。通过检查容易被PD-1抑制的基因和不容易被抑制的基因的表达模式,判断癌症特异性T细胞实际上多大程度被PD-1抑制,有望提前预测PD-1抑制剂抗体药的治疗效果。另外,容易被PD-1抑制的基因被认为可以作为癌症和自身免疫的治疗靶标。
论文信息
题目:PD-1 imposes qualitative control of cellular transcriptomes in response to T cell activation
期刊:《Molecular Cell》
DOI:10.1016/j.molcel.2019.12.012
文:JST客观日本编辑部编译