日本北海道大学遗传病调控研究所的北村秀光副教授与该校研究生院医学研究院的武富绍信教授等人组成的研究团队,成功查清了促进大肠癌转移的新控制机制,有望用来优化癌症免疫治疗。
在癌症恶化和复发的患者体内,负责消除癌细胞的抗肿瘤免疫细胞会功能失调。对于癌症治疗,控制复发和转移非常重要。但此前一直不太清楚体内免疫系统的癌症转移控制机制。
本研究通过建立大肠癌肝转移小鼠模型,对大肠癌细胞肝转移灶的形成与宿主免疫系统之间的关系进行了研究。研究发现,荷瘤小鼠体内产生的炎症性细胞因子之一IL-6会抑制抗肿瘤免疫,并促进大肠癌细胞转移灶的形成。研究还确认,在癌症环境下当IL-6缺损时,以PD-L1免疫抑制性分子为靶点的免疫检查点抑制疗法的抗肿瘤效果增强,肝转移模型小鼠的生存率显著提高。
今后有望利用这项研究成果,优化免疫检查点抑制疗法等癌症免疫治疗手段。
研究团队此前确认,荷瘤小鼠体内产生的IL-6会抑制树突状细胞的成熟和活化,会对导入抗肿瘤效应T细胞来消除癌细胞产生抑制作用(图1)。本研究明确了IL-6在抗肿瘤免疫与大肠癌复发和转移之间的关系,同时还尝试将其应用于新的癌症免疫疗法开发。
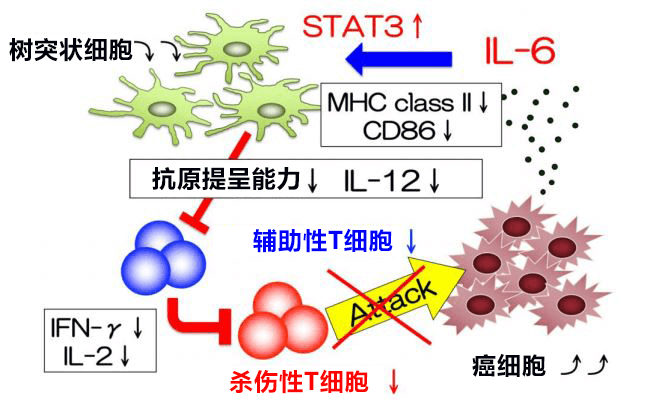
图1:荷瘤小鼠体内产生的IL-6作用于树突状细胞,抑制其抗原提呈能力和细胞因子的产生。由此导致辅助性和杀伤性T细胞等抗肿瘤效应细胞不能顺利工作,癌细胞无法从体内消除。
团队发现,与野生型大肠癌肝转移模型小鼠相比,IL-6缺陷小鼠的肝转移灶形成明显减弱;去除CD8阳性杀伤性T细胞后,抑制转移灶形成的效果会减弱。另外,IL-6缺陷时产生细胞毒性分子穿孔素和颗粒酶B的抗肿瘤效应T细胞及MHC II类会高表达;表达IFN-α/β和IL-12的成熟型树突状细胞以更高的频率向肝转移灶聚集;但同时通过抑制IFN-α/β受体及中和IL-12,会加剧本模型的肝转移灶形成。此外发现,向肝转移小鼠施用抗PD-L1抗体的免疫检查点抑制治疗后,与野生型相比,IL-6缺陷小鼠的生存率显著提高。
以上研究结果表明,荷瘤小鼠产生的IL-6会抑制树突状细胞的成熟和活化,导致抗肿瘤效应T细胞无法消除大肠癌细胞,从而促进大肠癌细胞肝转移灶的形成(图2)。今后有望通过抑制荷瘤小鼠产生的IL-6,来降低大肠癌的复发和转移。另外,通过控制IL-6还有望优化以免疫抑制分子PD-L1为靶点的免疫检查点抑制疗法(图 3)。
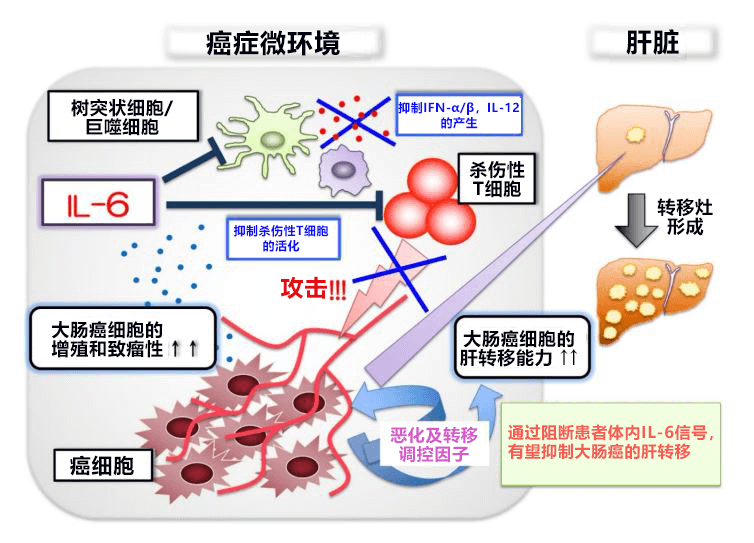
图2:在大肠癌肝转移模型中,IL-6通过抑制树突状细胞和巨噬细胞的细胞因子产生以及杀伤性T细胞的活化,来促进大肠癌细胞的增殖和肝转移灶的形成。因此,通过阻断IL-6信号,有望抑制大肠癌向肝脏的转移。
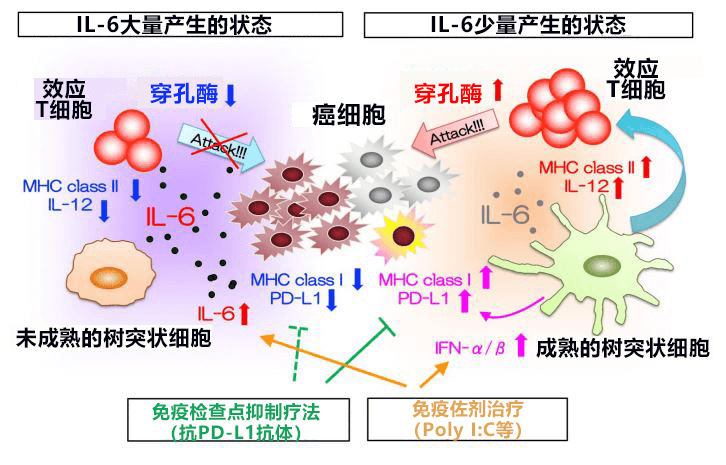
图3:在大量产生IL-6的状态下,免疫细胞被抑制,无法顺利攻击癌细胞。而在IL-6产生量较少的状态下,树突状细胞被激活,有望通过抗肿瘤效应T细胞攻击癌细胞。不过,在这种状态下会大量产生IFN-α/β,因此PD-L1分子表达增强,会加重癌细胞的免疫逃逸。因此,对IL-6较少的患者实施免疫检查点抑制治疗时,抑制IL-6和免疫检查点的联合治疗应更有效。另外,在除IFN-α/β外还会产生IL-6的免疫佐剂治疗中,阻断IL-6信号被认为比较有效。
论文信息
题目:IL6 Modulates the Immune Status of the Tumor Microenvironment to Facilitate Metastatic Colonization of Colorectal Cancer Cells
期刊:《Cancer Immunology Research》
DOI:10.1158/2326-6066.CIR-18-0766
文:JST客观日本编辑部翻译整理