发生于其他主要器官的癌经由血管或淋巴管转移到肺部,被称为转移性肺癌或者肺转移。日本东北大学研究生院医工学研究科肿瘤医工学领域的小玉哲也教授及Ariunbuyan Sukhbaatar特聘助教,与该校附属医院的讲师阪本真弥、森士朗等人的联合研究发现,传统的经血管递药系统在肺转移的超早期阶段没有疗效。
研究团队开发了可以重现目前的临床图像诊断系统检测不到的超早期肺转移病灶(100μm以下)的肺转移小鼠模型。利用微型X光CT进行解析发现,与正常的肺相比,肺转移模型的肺内总血管长度、总血管体积和总血管分支数量显著减少;病理组织图像显示,其原因在于肿瘤细胞阻塞了肺小动脉。这意味着,由于血管内的肿瘤堵塞,经血液递释的小分子抗癌化药不会充分到达肺转移灶。
已有动物实验表明,肿瘤新生血管特有的高通透性和滞留效应(Enhanced permeability and retention,EPR)会有效促进大分子药(10-200nm)向肿瘤聚集。但此次研究发现,模拟大分子药的荧光颗粒(直径145nm)并没有向肺转移灶聚集,即未发现基于肿瘤新生血管的EPR效应。
以上结果表明,在肺转移的超早期阶段实施经血管的全身化疗或靶向治疗时,不仅是小分子化药,大分子生物药也无法充分递送到肺转移病灶。
相关研究论文已于2019年11月5日发表在国际科学期刊《科学报告》(Scientific Reports)的网络版上。
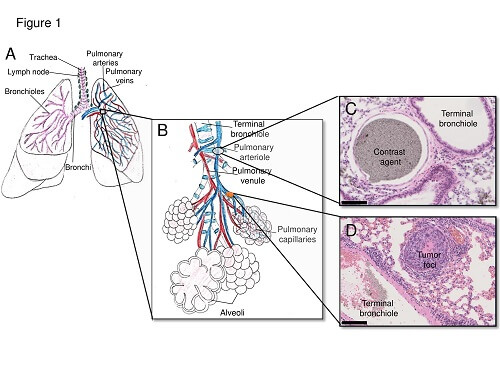
图1: 肺转移灶激活前后的肺小动脉变化。
(A)肺的解剖学结构和血管供应。(B)呼吸性细支气管的放大图,肺小动脉和静脉。(C、D)实施微型CT解析后对肺转移病灶进行苏木精-伊红染色。(C)的黑色椭圆表示肺部的正常结构,(D)中突出显示的橙色表示肿瘤病灶。比例尺为100μm。
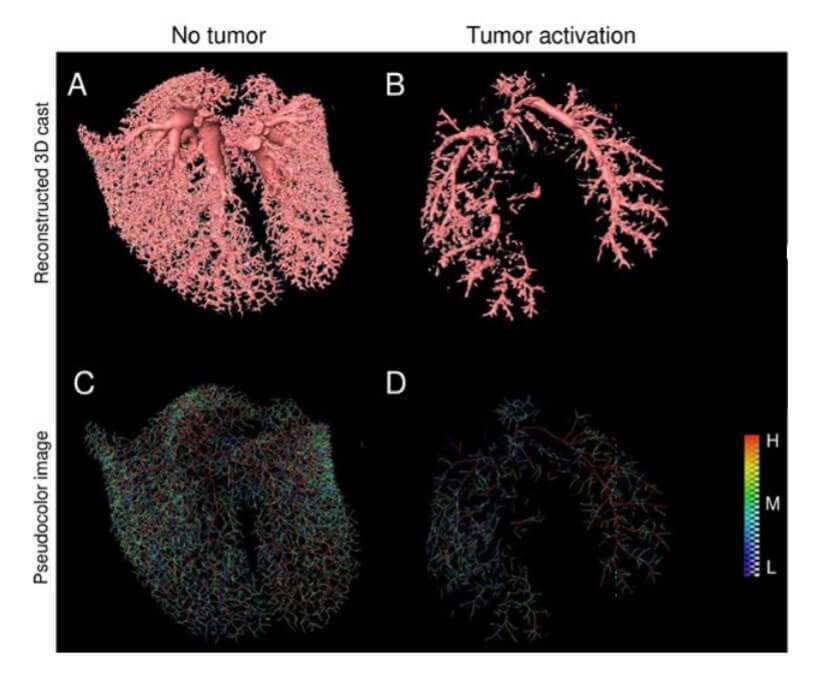
图2:肺部血管的重建图像。
(A和B)重建的肺部3D图像。
(C和D)肺部血管的伪彩色图像。血管颜色表示血管的粗细,用从蓝色(细,L)到红色(粗,H)的渐进色显示。
(A和C)普通小鼠的肺部血管新生。
(B和D)转移性肺部血管新生。肺转移病灶被激活后,肺小动脉被肿瘤细胞堵塞。
【论文信息】
题目: Analysis of tumor vascularization in a mouse model of metastatic lung cancer
发表期刊:《科学报告》(电子版)
DOI: 10.1038/s41598-019-52144-2
文:JST客观日本编辑部翻译整理