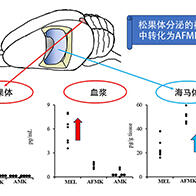
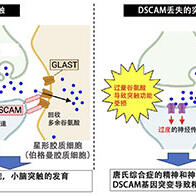
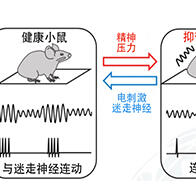
约70%的乳腺癌是雌激素受体(ER)阳性型,会大量产生与雌激素(女性荷尔蒙)结合促进癌症细胞繁殖的ER。因此,抑制雌激素发挥作用的内分泌疗法比较有效,但问题是在治疗过程中,基因在细胞中的被使用方式可能会发生变化,导致治疗无效,癌症复发。为解决这个问题,需要详细了解癌症基因组的DNA性质,尤其是立体结构,并查明复发型乳腺癌的特性,这在全球尚属于新推进的重要研究。
日本癌症研究会的齐藤典子等人组成的研究小组与熊本大学、九州大学和理化学研究所等开展联合研究,利用因长期实施的内分泌疗法失效而复发的乳腺癌模型细胞,调查了不产生蛋白质的非编码RNA分子Eleanor的作用。结果发现了一种看似矛盾的现象,即Eleanor会让用于细胞死亡的FOXO3基因和用于细胞繁殖的ESR1基因(产生ER的基因)立体接近,以便二者都可以被使用。
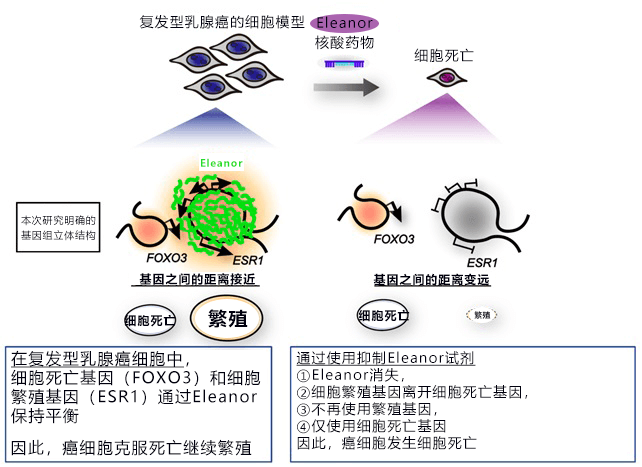
图1:癌细胞繁殖并杀死其他细胞示意图
使Eleanor消失的话,相互接近的基因会分离,ESR1基因不再在细胞内使用。另一方面,FOXO3基因仍然被使用,最终诱导细胞死亡。以上结果表明,癌细胞为躲避治疗环境继续繁殖,会利用Eleanor转换基因组的立体结构,并改变基因的使用方式,从而克服细胞死亡,这是此前未知的关于复发型乳腺癌的新机制。
以Eleanor为标靶的核酸药物和白藜芦醇会破坏基因被使用方式的平衡,诱导癌细胞死亡,因此有望用来治疗复发型乳腺癌。
相关研究成果已于2019年8月22日发布在自然出版集团的开放获取期刊《Nature Communications》上。
研究背景及经过
日本女性中大约每11个人就有1人罹患乳腺癌,位居女性癌症发病率之首,且患者数量呈增加趋势。约70%的乳腺癌是雌激素受体(ER)阳性型,会大量产生与雌激素(女性荷尔蒙)结合促进癌症繁殖的ER。因此,抑制雌激素发挥作用的内分泌疗法比较有效,但问题是会产生治疗抗性,导致治疗失去效果,癌症复发(图2)。
研究小组利用内分泌疗法失效的ER阳性乳腺癌模型细胞发现,不产生蛋白质的非编码RNA分子Eleanor会形成留在细胞核内的块状结构体(Eleanor Cloud),由此激活产生ER的ESR1基因,促进细胞繁殖。另外,为复发型乳腺癌模型细胞施用雌激素和类似药物白藜芦醇后,癌细胞会发生细胞死亡(图2)。因此研究认为,在复发过程中,乳腺癌细胞既具有繁殖能力,同时也具有容易发生细胞死亡的脆弱性。此前虽然一直期待这种性质能为治疗提供启发,但始终不清楚其详细机制。
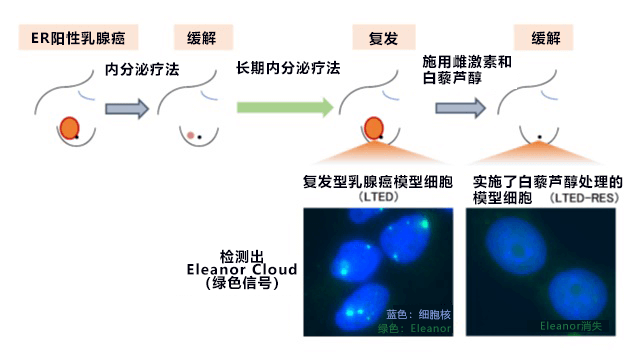
图2:乳腺癌存在复发问题
研究内容
此次,研究人员利用治疗失效的ER阳性复发型乳腺癌模型细胞(LTED细胞),抑制了Eleanor,并采用染色体构象捕获法解析了基因组的立体结构,同时还实施了调查基因使用方式的RNA-Seq解析。结果发现,复发型乳腺癌细胞积极利用了参与细胞死亡的FOXO3基因,宛若细胞已经准备好死亡一样。不过,研究人员还发现,参与繁殖的ESR1基因组区域以被Eleanor包围的形式接近FOXO3基因组区域,两者一同被激活。研究人员观察施用Eleanor抑制药物——白藜芦醇的细胞(LTED-RES细胞)发现,通过Eleanor接近的两个基因组区域的距离变得不稳定并越离越远,ESR1基因无法继续利用,但FOXO3基因仍然被使用,由此引起了细胞死亡(图3)。
同样,研究人员还调查了以Eleanor为标靶的核酸药物的效果。经确认,施用核酸药物与实施白藜芦醇处理具有相同的效果。Eleanor消失,FOXO3基因与ESR1基因的基因组区域分离,诱导了细胞死亡(图3)。核酸药物是目前备受关注的新一代抗癌药,由于与实施白藜芦醇处理相比能特异性地抑制Eleanor,预计副作用等比较少。因此,可能会成为今后值得期待的治疗药物。
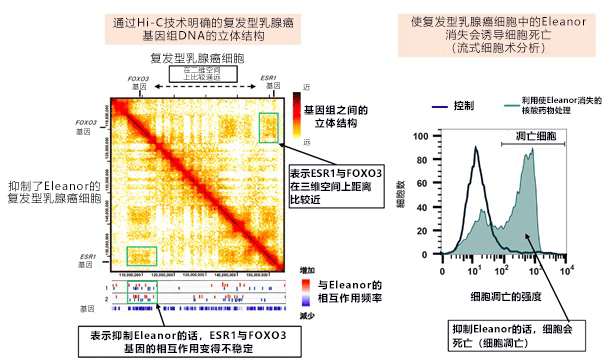
图3:FOXO3基因与ESR1基因的基因组区域分离,诱导细胞死亡
文:JST客观日本编辑部翻译整理