诺奖新闻发布会现场照片 (AFPBB News)
偶然发现“免疫抑制角色”可应用于癌症治疗
2018年诺贝尔生理学或医学奖授予了授予京都大学本庶佑教授和美国德州大学James P. Allison教授,以表彰他们在癌症治疗领域所做出的开辟性工作,使免疫疗法成为继手术、放射治疗和化学疗法之后的第四种癌症疗法。
本庶教授因为发现了免疫细胞表面的PD-1蛋白(Programmed Cell Death Protein 1)并阐明其功能和作用机理而获此殊荣。而PD-1蛋白最初的发现非常偶然。20世纪90年代初期,在本庶研究室攻读研究生的石田靖雄(现为奈良先端科技大学院大学副教授),一直在探索引起免疫细胞程序性死亡(即“细胞凋亡”)的因子。1992年他发现了第一个这样的因子,命名为PD-1(Programmed cell death-1)。
在通过小白鼠试验弄清其作用机制的过程中,有一些意外发现。在活性免疫细胞(T淋巴细胞和B淋巴细胞)中发现存在大量PD-1,而且被证明其具有抑制免疫应答的功能,可以担当“免疫抑制角色”(免疫检查点因子)。本庶佑在1999年发表了成果报告,同时他凭直觉感到,PD-1应该能够应用于感染症或癌症方面的治疗上。
自提出设想以来的半个世纪里,“免疫疗法”未能取得充分的成果
癌症免疫疗法,从提出设想至今已经历了半个世纪。1960年的诺贝尔奖得主、澳大利亚的免疫学者麦克法兰·伯内特(Macfarlane Burnet),在20世纪50年代提出了“癌症免疫监视学说”。这一学说认为,人体内每天会产生3,000个癌细胞,但人自身的免疫系统将之消灭,防止了癌症的发生。但长期以来,该现象未能得到证实。
支持这一学说的研究者们,开始积极研究开发通过免疫来控制癌症的治疗方法。但至今说不上已经取得了充分的成果。对于本庶佑来说,这也是个自然而然的发展过程。免疫应答,首先要识别抗原,这是关键(导火索)。只是,如果其中没有正向共刺激(激活)的作用,免疫细胞就不能充分活化。
以往的癌症免疫疗法,是找到癌症特异性抗原,将之置入人体内,以引发共刺激。但如果体内已有癌,并且抗原也肿大的情况下,仅仅加入数毫克的抗原,不会有明显效果。此外,如果施以负向共刺激(抑制)的话,不管怎么进行共刺激都引发不了免疫应答。如能解除这种抑制作用,使免疫细胞再度活化,将有助于治疗。关键点就在这里,本庶佑是第一位看透这一问题的免疫学者。
另一方面,美国德克萨斯大学的詹姆斯·阿利森(James Allison),也发现了另一个因子CTLA-4(cytotoxic T-lymphocyte-associated protein 4),同样对免疫细胞起抑制作用。1996年,他发表报告称,通过抗体阻碍CTLA-4发挥作用使得小白鼠的肿块消失了。
通过日美共同研究,确信“能开发出治疗药物”
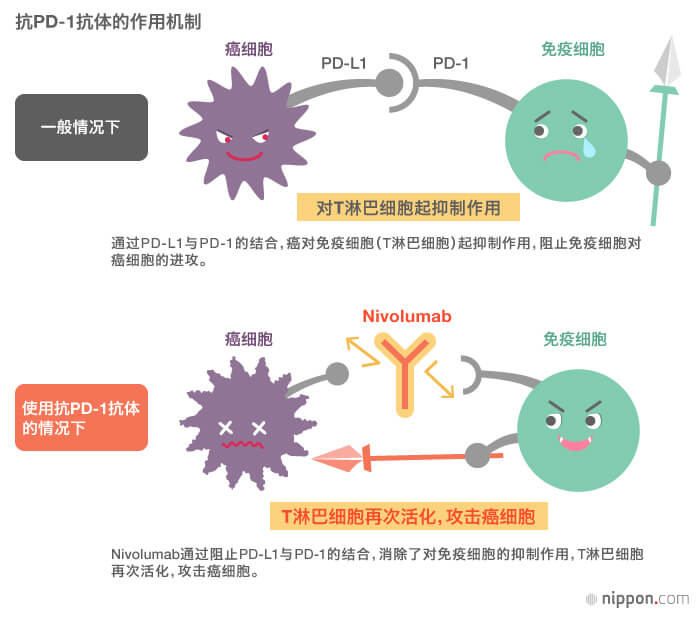
2000年,京都大学与美国遗传学研究所等机构联合开展研究,相继发现了能与PD-1进行特异性结合的物质(配体):PD-L1和PD-L2。癌细胞表面有PD-L1,其与免疫细胞的PD-1受体相结合的话,免疫细胞的反应就会被抑制,从而失去攻击癌细胞的能力。通过抗PD-1抗体阻止上述结合,就能消除对免疫细胞反应的抑制,免疫细胞就有可能再次攻击癌。
本庶研究室进行了动物实验,就像期待的那样,结果显示那些被投用了抗PD-1抗体的小白鼠,抗癌能力显著增强。2002年,本庶研究室发表了相关论文。另外,关于对移植的癌症转移的抑制作用,也通过各种实验补充了数据。
同时他们开始探索商用化的途径,但由于当时的京都大学申请专利经验不足,本庶佑邀请与其老师早有交往的小野药品工业公司联合申请专利。2002年,他们递交了将PD-1用于免疫治疗用途专利的临时申请案。
本庶佑坚信,抗PD-1抗体能成为治癌药物,他向很多制药企业提议开发新药。但在早期,包括小野药品工业公司在内,对于癌症免疫疗法都持怀疑态度,所以一直没能得到积极的回应。本庶佑看到在日本国内基本没戏,于是转而寻求与美国的风险投资企业合作,美方反应十分积极。本庶把这一情况告知了小野药品工业公司,小野药品终于在最后关头答应了自己来开发新药。事实上,美国的生物技术企业Medarex公司,拥有制造人类抗体的专利,曾和小野药品工业公司接触,希望能将PD-1抗体推向临床应用。这是小野药品工业公司最后改变想法的根本原因。
2006年,美国食品药品监督管理局(FDA)批准,Nivolumab作为人类PD-1抗体,可作为研究用途的新药,同年在美国开展临床试验。2009年,美国制药巨头百时美施贵宝公司,以24亿美元的价格收购了Medarex公司,新药研发进一步加速。
2014年,癌症治疗药物“Opdivo”诞生
在美国开展的临床试验中,以非小细胞性肺癌、前列腺癌、大肠癌、肾癌等固形癌以及恶性黑色素瘤为对象,实施了投药试验,所有试验都确认有疗效。结果显示,对于黑色素瘤和肾癌,近30%有疗效(是指癌消失了或者癌缩小了一定比例之上的人所占的比例)。2012年在最权威的临床医学杂志《新英格兰医学杂志》上发表了有关实验结果的报告。有评论认为,这是“过去30年中尝试过的众多癌免疫疗法中,具有最高疗效的”。有些患者甚至长期(一年以上)没有再复发。
在日本,小野药品工业公司以非小细胞性肺癌、肾癌等患者为对象,开展了安全性调查的第一阶段试验。有些病例显示疗效显著。其中,先期以预想疗效最差的黑色素瘤为对象进行新药开发。实际上,在日本国内,实施以黑色素瘤为对象的第二阶段试验,是时隔20年之后的第一次。
这种使用抗体的“癌症免疫疗法”,被美国科学类杂志《Science》评选为2013年的“年度突破(Breakthrough of the Year)”之一。2014年7月,Nivolumab以“Opdivo”的形式,率先在日本获准用于黑色素瘤的治疗,9月美国也获得通过。将其用于肺癌(有过治疗经历、处于发展期的扁平上皮肺癌)的治疗方面,在美国已经结束了试验阶段,进入优先审批环节。
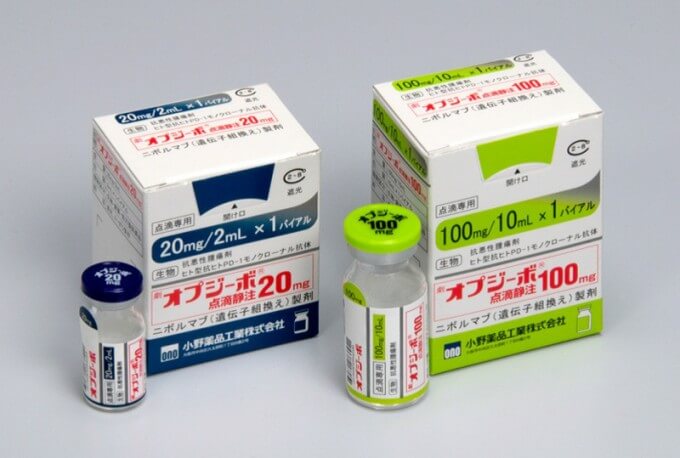
小野药品工业公司研制的“Opdivo”(摘自该公司新闻稿)
现在,正在针对多种癌症实施临床试验,预计将依次适当扩大试验范围。而且,世界上众多制药企业,正在以“免疫检查点”为靶标研发多种新药。
2011年,百时美公司的抗CTLA-4抗体Ipilimumab,获得美国FDA批准(在日本的审批还在申请中)。CTLA-4和PD-1一样,都是免疫检查点因子,为了消除对免疫反应抑制的不同方面,同时使用这两种药物能够大幅改善药效。本庶佑和阿利森被评选为2014年度“唐奖”(Tang Prize)生技医药部门的首届获奖者(奖金5千万台币,相当于约1.7亿日元)。唐奖创设于台湾,有“东方诺贝尔奖”之称。

本庶佑(左)出席台湾创设的“唐奖”(Tang Prize)颁奖仪式。2014年9月18日摄于台湾台北市内(图片提供:财团法人唐奖教育基金会)
有诸多优点如“副作用小”,但治疗费用高昂
和传统抗癌药物相比,Nivolumab有以下几个突出特点:①可针对任何癌症;②副作用小;③即便是癌症晚期,如果一开始有疗效的话,就能一直有效,可以多次投药。这与以特定类型癌症的增殖有关的因子为专门目标的因子靶标药物相反,阻碍免疫检查点类药物能成为治疗各种类型癌症的广谱药物。本庶佑预测说,“不久的将来,现在的抗癌药物几乎都将不再使用,所有的癌症都会用PD-1抗体来治疗吧”。
但其最大的劣势,就是价格昂贵。一位患者一年的治疗费用,据说平均高达约1500万日元。不过,其他的因子靶标药物也很贵,而且它们无法应对癌细胞的变异,这样很快就会失效。但是,使用了Nivolumab的患者中,有很多人的癌细胞全部或部分消失了,显示出了良好的疗效,从性价比来讲,Nivolumab也并非贵得离谱。在日本,如果适用保险的话,患者作为高额疗养费制度的对象,其自费负担可以轻减。但对于政府困窘的保险财政来说,则将成为沉重的负担。
剩下的大课题就是,在有些患者身上可以达到无需再用药程度的显著效果,但同时也有人完全没有疗效。作为应对措施,应尽量早期使用,同时也在计划开发能够用来预先测定有否疗效的试剂。
有必要构建基础与临床、大学与企业之间的“良性循环”机制
关于Nivolumab,不仅最初的原型,就连检验产品概念可行性的初期临床试验(POC测试)的创意,也是在大学里诞生的。由于从基础到临床的“接力”研究进展顺利,才结出了果实。
作为“安倍经济学”第三支箭(促进民间投资的经济增长战略)的重要举措,日本医疗研究开发机构(AMED)4月1日成立了。以iPS细胞(诱导性多功能干细胞)为代表,日本的基础研究水准并不低于国外,但将研究成果转变成临床应用的体制却很薄弱。日本医疗研究开发机构这个组织,全盘掌握医疗领域的研究开发预算,根据研究的进展情况促进研究成果的商用化。据说是仿照美国的国立卫生研究所(NIH)创办的。
本庶佑曾在美国NIH做过研究工作。他指出,“日本的医疗创新是‘单程车票’,政策很不完备”。“有必要建立使制药企业获取的利润反哺大学的机制,这样才能形成人才辈出、创新不断的良性循环”。通过与有国际竞争力的制药企业形成真正的双赢关系,期待能够早日救护那些因癌症就快要失去生命的人们。
2018年10月2日,诺贝奖公布的第二天,本庶佑宣布将把获得的约5750万日元奖金全部捐给母校京都大学,设立基金,资助生命科学领域的年轻研究人员。
作者 塚崎朝子
原文转载自日本网[网址]
由客观日本编辑部编辑修改