【日本药品监管体系(二)】医药生活卫生局
作为日本厚生劳动省的内部部局之一,医药生活卫生局的主要职能除了确保药品、准药品(功能性食品、药用化妆品等)、化妆品、医疗器械等的有效性和安全性以及医疗单位的安全运行之外,还涵盖与国民生活健康息息相关的各类问题,如食品和饮水卫生、血液管理、毒品和兴奋剂管控、药剂师国家考评等。

2001年1月6日,原厚生省和原劳动省合并时,原厚生省医药安全局更名为医药食品局。
2015年10月1日,为应对严峻的老龄化步伐,追求延长国民健康寿命、提高人民生活质量、建立可持续社会保障体系的目标,厚生劳动省内部进行了系列改组。其中,健康局的生活卫生科和供水科正式划入医药食品局的食品安全部;同时,食品安全部改称“生活卫生与食品安全部”,医药食品局则变更为“医药生活卫生局”。健康局则由原有的“癌症控制和健康促进”、“疾病控制”、“结核感染症”三个科室改组为“健康”、“癌症和疾病控制”、“顽疾对策”、“结核感染症”四个科室。
生活卫生与食品安全部在此不展开讨论,医药部分主要由局长、医药秘书处以及下列5个职能部门负责具体实施(图1)。

图1 医药生活卫生局组织架构(日本制药工业协会官网)
总务科主要负责医药生活卫生局各类综合事务、药剂师相关事务,以及其他四部门职责外与PMDA(医药品医疗器械综合机构)的相关对接工作。总务科下辖医药品不良反应损害对策室,顾名思义,主要处理医药品等造成的健康损害等问题,以及针对PMDA医药品不良反应损害救济制度和生物制品感染等损害救济制度等相关工作(图2)。医药生活卫生局职责内的国际相关事务则归国际药事规则室对应。
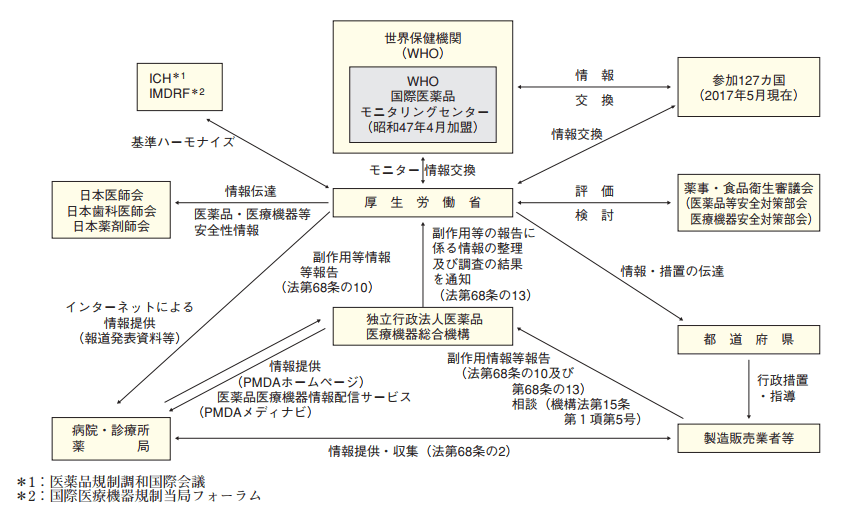
图2 不良反应报告制度概略(厚生劳动白皮书)
医药品审查管理科具体负责医药品基准、孤儿药指定、制造贩卖许可认证、生产指导监督、上市后的再审查等相关工作外(图3),还需要对接药局方(不同于兼卖日用品和一般OTC药品的药妆店,药局是必需有药剂师和能销售处方药的药店)以及PMDA药品制造贩卖相关的业务。
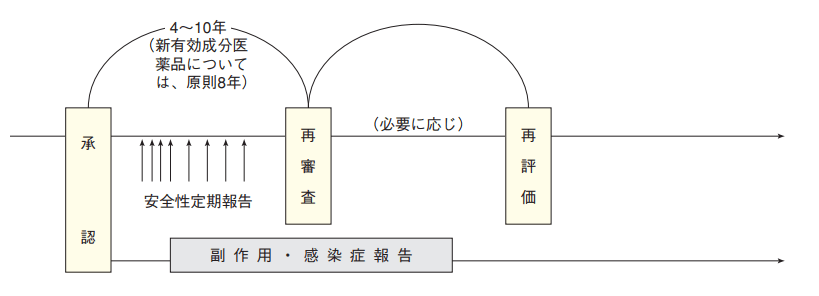
图3 医药品上市后再审查与再评估流程 (厚生劳动白皮书)
对应地,医疗器械、体外诊断试剂、再生医疗制品等的基准制定、工业标准的准备和推广、产品登录、制造贩卖许可认证、生产指导监督、上市后再审查等属医疗器械审查管理科(图4)。同时,该科还需负责医疗器械和体外诊断试剂的实际使用成绩评价、与器械销售和售后服务商以及再生医疗制品提供商等相关工作。
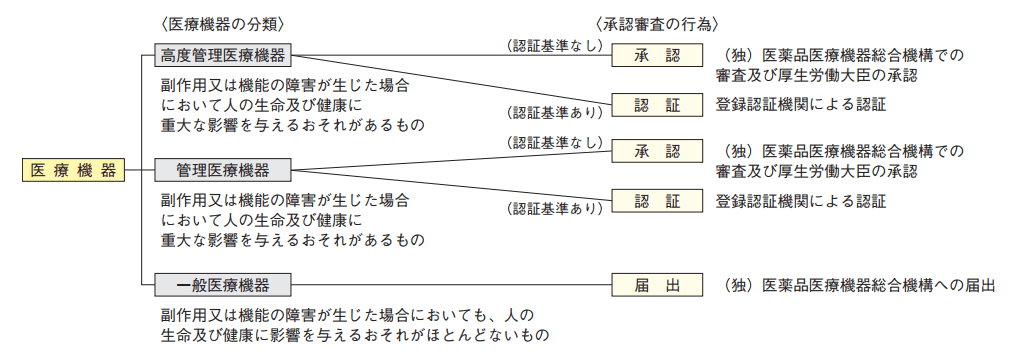
图4 医疗器械上市审批审查机制(厚生劳动白皮书)
医疗器械审查管理科下属化学物质安全对策室,主要负责有毒有害物质(监视指导与毒品对策科职责范围以外部分)、含有有毒成分的家居用品、二噁英等的管控,以及对可能危害人类健康或动植物栖息环境的化学物质的评估、制造、进口、使用等的管理。
医药安全对策科主要确保医药制品和医疗器械等安全性的企画、立案、调查,督导生物制品和特殊医疗器械记录作成及保管等文书工作,以及负责与PMDA安全性业务的对接。
监视指导与毒品对策科,负责对误导宣传或者假冒伪劣医药制品及医疗器械的取缔、药品广告的指导监督、医药品检查检定及PMDA实施的现场检查协助、毒品及兴奋剂等的取缔和相关国际合作,以及药事监督员、毒品取缔官及毒品取缔员的管理等。
血液对策科的职责包括采血监督、献血推进、血液制剂的稳定供给和正确利用(图5),以及生物制剂生产流通的改善和调整(健康局职责以外部分)。
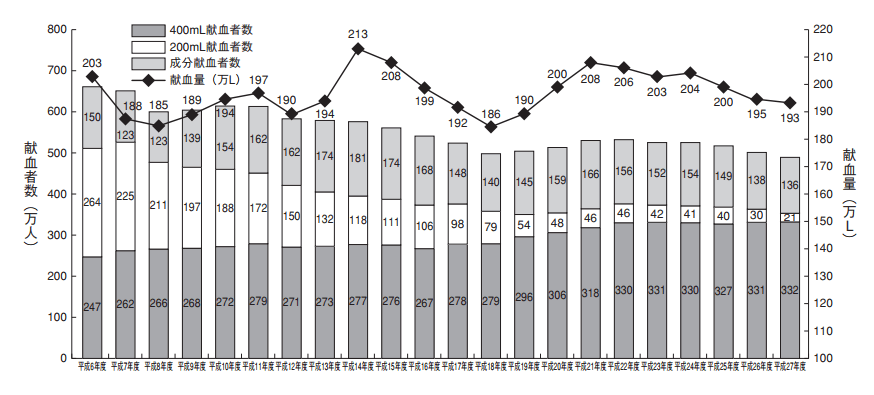
图5 不同种类采血人数推移(厚生劳动白皮书)
供稿 宋傑
编辑修改 客观日本编辑部
相关链接:
厚生劳动省官网 [网址]




























